Patientenbezogener Medikationsplan
|
|
Dieses Dokument gibt wieder:
Implementierungsleitfaden Patientenbezogener Medikationsplan (1.00). Die Teilmaterialien gehören der Kategorie cdamedp an. |
auf Basis der HL7 Clinical Document Architecture Release 2 für das deutsche Gesundheitswesen
HL7 Deutschland
Dr. Kai U. Heitmann
| Version: | 1.00 |
| Datum: | 3. August 2017 |
| Status: | |
| Verfahren: | {{{Verfahren}}} |
| Realm: |
| Abstimmungsdokument | |||
|---|---|---|---|
| Version | Datum | Status | Realm |
| 0.90 | 06.01.2015 | ||
| [download] | |||
| 0.97 | 03.03.2015 | ||
| [download] | |||
| 1.00 | 03.08.2017 | Angenommen | |
| [download] | |||
| Kontributoren | ||
|---|---|---|

|
Viktor Krön, Ärztekammer Nordrhein | Düsseldorf |
| Ärztekammer Westfalen-Lippe | Münster | |
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Inhaltsverzeichnis
- 1 Dokumenteninformationen
- 2 Einleitung
- 3 Struktureller Aufbau
- 4 Terminologien
- 5 Appendix (nicht normativ)
- 6 Referenzen
- 7 Abbildungsverzeichnis
Dokumenteninformationen
Impressum
Dieser Leitfaden ist im Rahmen des Projekts „Medikationsplan 2.0 Plus“ des Landes Nordrhein-Westfalen zusammengestellt und unterliegt dem Abstimmungsverfahren des Interoperabilitätsforums und der Technischen Komitees von HL7 Deutschland e. V.
Ansprechpartner
- Dr. Kai U. Heitmann, HL7 Deutschland e.V., Heitmann Consulting and Services
- Prof. Dr. Sylvia Thun, Hochschule Niederrhein, Krefeld
- Viktor Krön, Ärztekammer Nordrhein
- Thomas Althoff, Ärztekammer Westfalen-Lippe
- Dr. Christof Geßner, HL7 Deutschland e.V.
- Dr. Frank Oemig, Agfa HealthCare GmbH
- Mathias Aschhoff, ZTG GmbH
Disclaimer
- Der Inhalt dieses Dokumentes ist öffentlich. Zu beachten ist, dass Teile dieses Dokuments auf der Normative Edition 2005 von HL7 Version 3 beruhen, für die © HL7 International gilt.
- Obwohl diese Publikation mit größter Sorgfalt erstellt wurde, kann HL7 Deutschland keinerlei Haftung für direkte oder indirekte Schäden übernehmen, die durch den Inhalt dieser Spezifikation entstehen könnten.
Autoren
- Dr. Kai U. Heitmann, HL7 Deutschland e.V., Heitmann Consulting and Services
Copyright-Hinweis, Nutzungshinweise
Die Nachnutzungs- bzw. Veröffentlichungsansprüche sind nicht beschränkt.
Der Inhalt dieser Spezifikation ist öffentlich.
Der Patientenbezogene Medikationsplan (PMP) basiert auf dem national adaptierten HL7-Standard der „Clinical Document Architecture (CDA)".
Näheres ist unter http://www.hl7.de und http://www.hl7.org zu finden. Für alle veröffentlichten Dateien mit einem CDA-Bezug gilt ferner: Alle abgestimmten und veröffentlichten Spezifikationen wie Implementierungsleitfäden, Stylesheets und Beispieldateien sind frei verfügbar und unterliegen keinerlei Einschränkungen, da die Autoren auf alle Rechte, die sich aus der Urheberschaft der Dokumente ableiten lassen, verzichten.
Die im Anhang genannten Ausführung zu anderweitigen Lizenzen sind zu beachten.
Alle auf nationale Verhältnisse angepassten und veröffentlichten CDA-Schemas können ohne Lizenz- und Nutzungsgebühren in jeder Art von Anwendungssoftware verwendet werden.
Aus der Nutzung ergibt sich kein weiter gehender Anspruch gegenüber HL7 Deutschland oder den Autoren, zum Beispiel eine Haftung bei etwaigen Schäden, die aus dem Gebrauch der Spezifikationen bzw. der zur Verfügung gestellten Dateien entstehen.
Danksagung
Wir danken besonders
- der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ)
- der Ärztekammer Nordrhein
- der Ärztekammer Westfalen-Lippe
- dem Land Nordrhein-Westfalen
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Einleitung
Rationale
Der Patientenbezogene Medikationsplan (PMP) ist eine umfassende und im Idealfall vollständige Aufzeichnung der Medikamente des Patienten (Verordnungen, nicht verschreibungspflichtige Medikamente, Kräuterprodukte, Nahrungsergänzungsmittel und andere). Der vorliegende Implementierungsleitfaden stellt die vereinheitlichte elektronische Wiedergabe derartiger Medikationspläne dar und bildet den offiziellen CDA-basierten Medikationsplan in ISO/HL7 27932:2009 Fassung für Deutschland.
In einem Sondergutachten[1] fordert der Sachverständigenrat zur Begutachtung der Entwicklung im Gesundheitswesen 2012 einen vollständigen Überblick über die Arzneimittelhistorie des Patienten als Information zur eigenen Medikation durch einen einheitlichen Patientenbezogenen Medikationsplan.
99. Bei der Verbesserung der sektorenübergreifenden Kommunikation zur Sicherstellung von Versorgungskontinuität spielt die sektorenübergreifende
Arzneimitteltherapie eine herausgehobene Rolle. (...) Zur Gewährleistung einer sektorenübergreifenden Versorgung im Bereich der Arzneimitteltherapie
müssen folgende Voraussetzungen erfüllt sein:
a) Der behandelnde Arzt muss einen vollständigen Überblick über die Arzneimittelhistorie des Patienten haben. Dazu gehören vollständige Angaben über alle aktuell eingenommenen Arzneimittel inklusive frei verkäuflicher (Over the Counter) Medikamente und im Einzelfall auch solche, die früher eingenommen wurden.
Zielsetzung
Der Patient und der sichere Umgang mit seinen Medikamenten steht eindeutig im Vordergrund Patientenbezogener Medikationspläne. Zusätzlich können (sollen) hier auch Informationen für Gesundheitsdienstleister enthalten sein, die die Arzneimitteltherapiesicherheit erhöhen:
- Informationen für den Patienten: die patientengerechte Darstellung aller häufigen Einnahmesituationen steht im Vordergrund, damit Compliance und Einnahmesicherheit erhöht werden
- Informationen für Gesundheitsdienstleister: die Arzneimitteltherapiesicherheit soll erhöht werden, indem die oben genannten Angaben und ggf. Zusatzinformationen wie Körpergewicht im Prinzip jedem an der Therapie beteiligten Gesundheitsdienstleister wie z. B. Ärzten oder Apothekern zur Verfügung stehen.
Der Plan soll das Ergebnis der Zusammenarbeit von Patient, Arzt, Apotheker und anderen Gesundheitsdienstleistern sein.
Hintergründe
Im Rahmen eines Workshops im BfArM am 5. Mai 2011 (vgl. auch [2]) wurden die Inhalte des einheitlichen Medikationsplans umrissen:
- Basisinformationen
- Datum
- Kontaktdaten des Ersteller
- Patientenstammdaten
- Informationen zum Arzneimittel
- Wirkstoff
- Arzneimittelname
- Darreichungsform (ggf. Anwendungsart)
- Wirkstärke
- Informationen für den Patienten
- Relevante Anwendungs- und Einnahmehinweise – optional
- Zusätzliche Hinweise (Lagerung und Aufbewahrung) – optional
- Informationen zur Therapie
- Behandlungsgrund (für den Patienten verständlich) – optional
- Therapiezeitraum: Beginn / Dauer / Ende – optional
- Bedarfsmedikation (ja/nein)
- Dosierschema
Im Allgemeinen enthalten solche Pläne daher folgende Komponenten (siehe auch [3] [4] [5] [6]):
| Informationsblock | Informationen für den Patienten | Zusätzliche Informationen mit Fokus auf die Gesundheitsdienstleister |
|---|---|---|
| Angaben zum Patienten |
|
|
| Klinische Parameter |
|
|
| Datum und Identifikation |
|
|
| Medikation |
|
|
| Wichtige Hinweise | ||
| Unterschriften | Patient | Arzt |
Vorgaben der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ)
Die Vorgaben des Medikationsplans der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) Version 2.0[7] sind als ein führender Ausgangspunkt für den vorliegenden Implementierungsleitfaden gewählt. Grundsätzlich lassen sich mit der hier vorliegenden Spezifikation darüber hinaus auch andere Medikationspläne abbilden, wie sie hierzulande beispielweise an verschiedenen Standorten in Erprobung oder Routine befindlich sind [8].
Projekte zum Medikationsplan Plus
Im Rahmen des Projekts „Medikationsplan 2.0 Plus“ in Nordrhein-Westfalen, gefördert durch die Ärztekammern Nordrhein und Westfalen-Lippe sowie das Ministerium für Gesundheit, Emanzipation, Pflege und Alter des Landes Nordrhein-Westfalen, Düsseldorf, stehen dazu im Fokus
- Verbesserung der Patienteninformation und -compliance
- Patientengerechte Darstellung aller häufigen Einnahmesituationen
- Möglichkeit der Angabe von zeitlich limitierten Einnahmevorschriften (Startdatum und Dauer z. B. in Tagen, bzw. Stopdatum)
- Möglichkeit der Angabe aller vom Patienten eingenommenen Präparate, also auch OTC (over-the-counter) Präparate wie z.B. Multivitamin-Präparate oder die Selbstmedikation des Patienten (nach Auskunft des Patienten oder eines Angehörigen etc.)
- Verbesserung der Arzneimitteltherapiesicherheit
- Transparenz der Medikation
- Verbesserung der intersektoralen und interprofessionalen Kommunikation
- Interoperabilität und Erweiterbarkeit (eArztbrief)
- Kommunikation mit dem europäischen Nachbarn (Österreich, Niederlande)
- Bereitstellung von XSL-Stylesheets und einer zugehörigen bijektiven Abbildung von CDA-Instanzen in ein Kurzformat, z. B. für die Unterbringung in Barcodes oder auf anderen kapazitätslimitierten Träger (siehe auch Abschnitt "Abgrenzung").
Vorarbeiten
Der vorliegende Implementierungsleitfaden berücksichtigt eine Reihe von Vorarbeiten aus dem nationalen und internationalen Umfeld.
- Die Vorgaben des Medikationsplans der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) Version 2.0[7] sind ein führender Ausgangspunkt gewählt; nichtsdestoweniger gibt es hier kritische Anmerkungen vor allem zur technischen Umsetzung, siehe hierzu Appendix "Kritische Anmerkungen zur Spezifikation des Medikationsplans der AkdÄ".
- CDA Implementierungsleitfaden für einen patientenbezogenen Medikationsplan. Dr. Jörg Caumanns, Dr. Andreas Billig // Fraunhofer FOKUS Auftraggeber: Deutsche Krankenhausgesellschaft e.V., 2014[9]
- Vorarbeiten von HL7 Deutschland zum Thema "Medikationsplan" (z. B. von Frank Oemig und Christof Gessner, siehe auch [10])
- Die einschlägigen inhaltlichen IHE-Profile (PRE, DIS, PADV, PML)[11], insbesondere das Template "Medications" 1.3.6.1.4.1.19376.1.5.3.1.4.7 im Rahmen des Technical Framework "Patient Care Coordination (PCC)" von IHE [12]
- Vorarbeiten aus dem österreichischen ELGA-Umfeld: ELGA Implementierungsleitfaden: HL7 Implementation Guide for CDA® R2: e-Medikation. Zur Anwendung im österreichischen Gesundheitswesen [1.2.40.0.34.7.8.1], 2014 (Leitfäden siehe elga.gv.at[13]; Spezifikation in ART-DECOR[14])
- Teilprojekt "Prescription" aus dem epSOS-Projekt[15], Spezifikation in ART-DECOR[16]
- Arztbrief des VHitG (jetzt bvitg) 2006[17]) und das Addendum "Medikation", 2007;
- eArztbrief 2014, definiert und abgestimmt durch das Interoperabilitätsforum im Dezember 2014[18]
- CDA-CH-SMTL shared medication treatement list, Genf[19]
Bei IHE ist das am ehesten ähnliche Profil die "Medication List" (PML). Dies ist als Sammlung von Verordnungen und Abgaben von Medikamenten konzipiert. Die hier vorliegende Spezifikation des Medikationsplans klassifiziert das Dokument im Gegensatz dazu als Personenbezogene Medikationsliste (Personal Medication List), Referenzen auf Verordnungen oder Abgaben sind nur optional.
Diese Ergänzung zu den bisherigen Profilen wurde auch in den Synchronisationsprozess mit den IHE Profilen "Pharmacy Medication List" und "Medication Treatment List" der gemeinsamen HL7 und IHE Pharmacy Gruppe eingebracht und wird dort entsprechenden Niederschlag finden.
Abgrenzung
Dieser Leitfaden deckt eine Reihe von Themen nicht ab. Dazu gehören:
- Prozessbeschreibung
- Use Cases
- Digitale Signatur (siehe auch Abschnitt "Digitale Signatur")
- Security
- Transport von CDA-Dokumenten
- Verwendung von XSL-Stylesheets
- Ultrakurzformat XML zum Einsatz für kapazitätslimitierte Datenträger[20]
- Datenschutzrechtliche Bewertungen
XSL-Stylesheets und Ultrakurzformat XML
Im Rahmen der Projekts zum Medikationsplan in Nordrhein-Westfalen wird ein XSL-Stylesheet und ein Ultrakurzformat XML zum Einsatz für kapazitätslimitierte Datenträger entwickelt und erprobt. Das Stylesheet wird benutzt, um die beschriebenen Inhalte des Medikationsplans in der empfohlenen Form durch automatisierte Transformation visuell darzustellen. Im Rahmen dieses Projekts wurde auch ein XML-Ultrakurzformat für den Medikationsplan entwickelt, welches für kapazitätslimitierte Datenträger (wie zum Beispiel Barcodes) eingesetzt werden kann. Das Format ist als bijektive Abbildung zu sehen, das heißt aus einer CDA-Version nach der hier beschriebenen Spezifikation (Langfassung) kann die Ultrakurzfassung mittels einer Transformation generiert werden und umgekehrt.
Als Ergebnis aus dem NRW-Projekt und im Anschluss an die Abstimmung, Überarbeitung und endgültige Verabschiedung der vorliegenden Spezifikation werden XSL-Stylesheet und Ultrakurzformat bereitgestellt.
Digitale Signatur
Im Rahmen des NRW-Projekts wird die digitale Signatur wie in [21] beschrieben verwendet. Auf die Verwendung von Signaturen wurde im Rahmen des Arztbriefs bereits 2010 hingewiesen (vgl. [22]).
Zum Zwecke der Signatur sind in diesen Leitfaden die in CDA üblichen Mechanismen aufgenommen, die digitale Signaturen ermöglichen bzw. hierfür als notwendig erachtet werden. Dies betrifft die Verwendung von Elementen zur Wiedergabe von Unterzeichnern (legalAuthenticator, authenticator) im Header.
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Struktureller Aufbau
Verwendeter Standard
In der vorliegenden Spezifikation des Patientenbezogenen Medikationsplans ist die Clinical Document Architecture Release 2 (CDA R2), auch ISO/HL7 27932:2009 die Grundlage.
Verbindung von funktionaler Beschreibung und CDA Strukturen
Die im vorigen Abschnitt beschriebenen Angaben zur Struktur eines Medikationsplans (funktionale Beschreibung) sind in einem Datensatz zusammengefasst und in ART-DECOR[23] dokumentiert.
|
Patient 1..1 M
100
Klinische Parameter 1..1 R
200
Ersteller 1..1 M
300
Medikationseintrag 0..* R
400
Sonstiger Hinweis 0..1 R
600
Identifikation 1..1 R
500
|
[Abbildung 1] Übersicht zur funktionalen Beschreibung des Patientenbezogenen Medikationsplan, siehe auch ART-DECOR für Details
Damit ist eine Verbindung zwischen der Sicht der Anforderungen des Gesundheitsdienstleiters (definiert z. B. durch die Koordinierungsgruppe der Arzneimittelkommission der deutschen Ärzteschaft) in der Form der funktionalen Beschreibung einerseits und der technischen Strukturen wie CDA Header und Body und den zugehörigen Templates andererseits möglich. Der Bezug zwischen den hier spezifizierten Templates und der funktionalen Beschreibung wird im Folgenden angegeben durch Verweise auf die Konzepte in der Form 'Ziel der Konzept Id(s): ... ', wobei die Konzept Id(s) sich auf die in der ART-DECOR-Variante der Spezifikation hinterlegten funktionalen Konzepte bezieht.
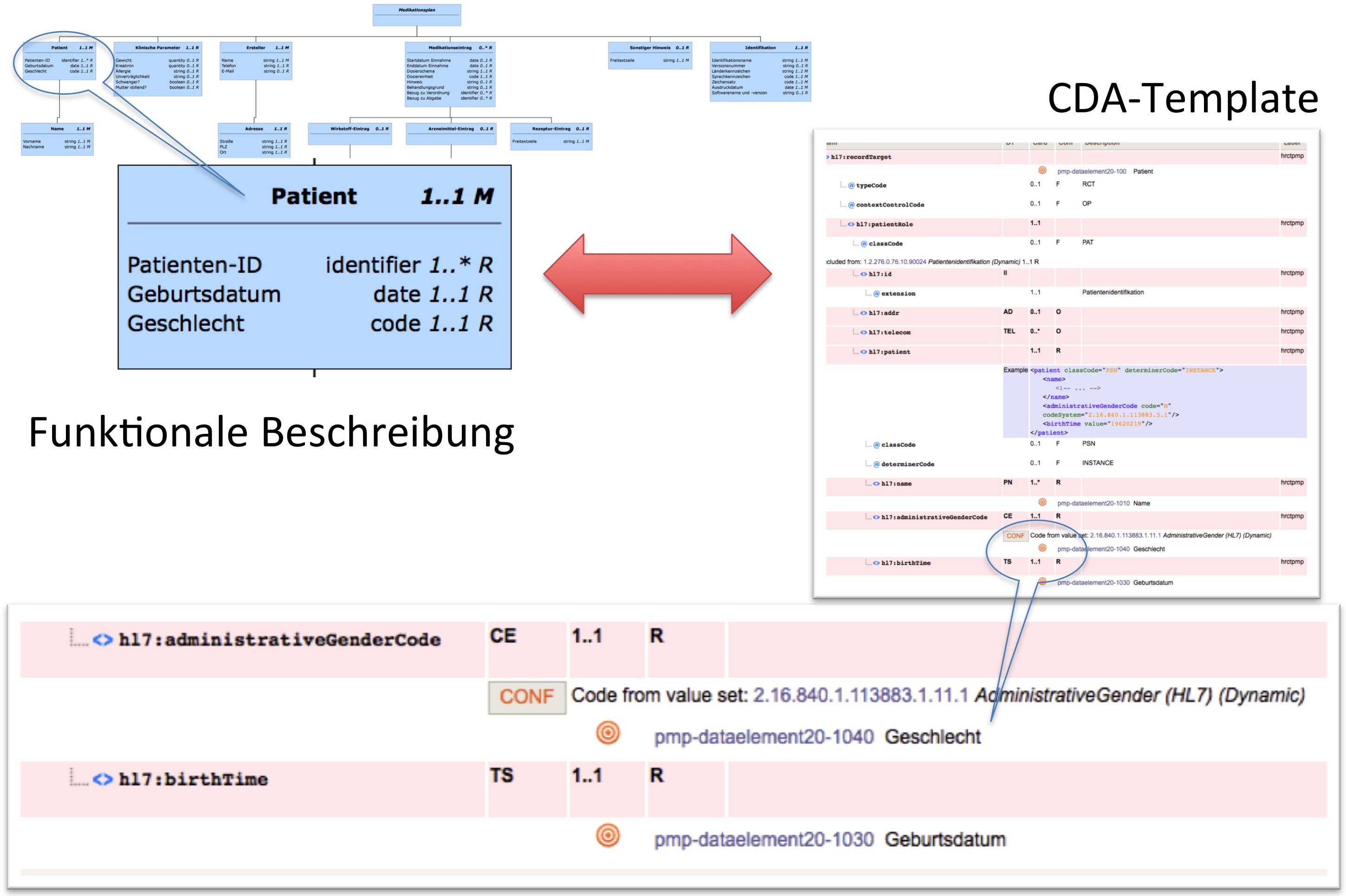
[Abbildung 2] Zusammenhang zwischen funktionaler Beschreibung und technischer Spezifikation
Übersicht CDA Header und Body
Auf der Basis der oben beschriebenen Angaben und der Spezifikation des Medikationsplans der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) Version 2.0[7] hat der hier spezifizierte Patientenbezogene Medikationsplan folgende Grobstruktur nach CDA:
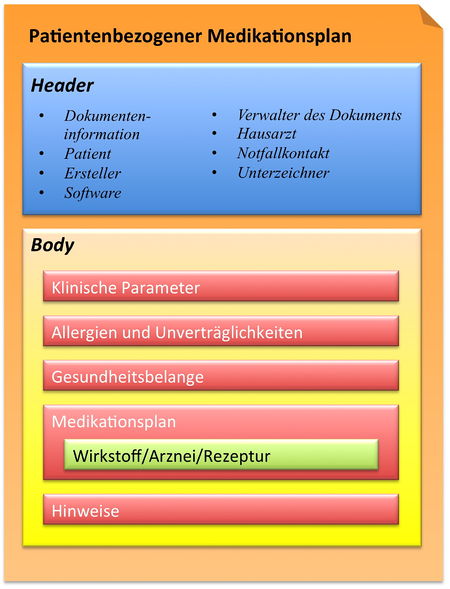
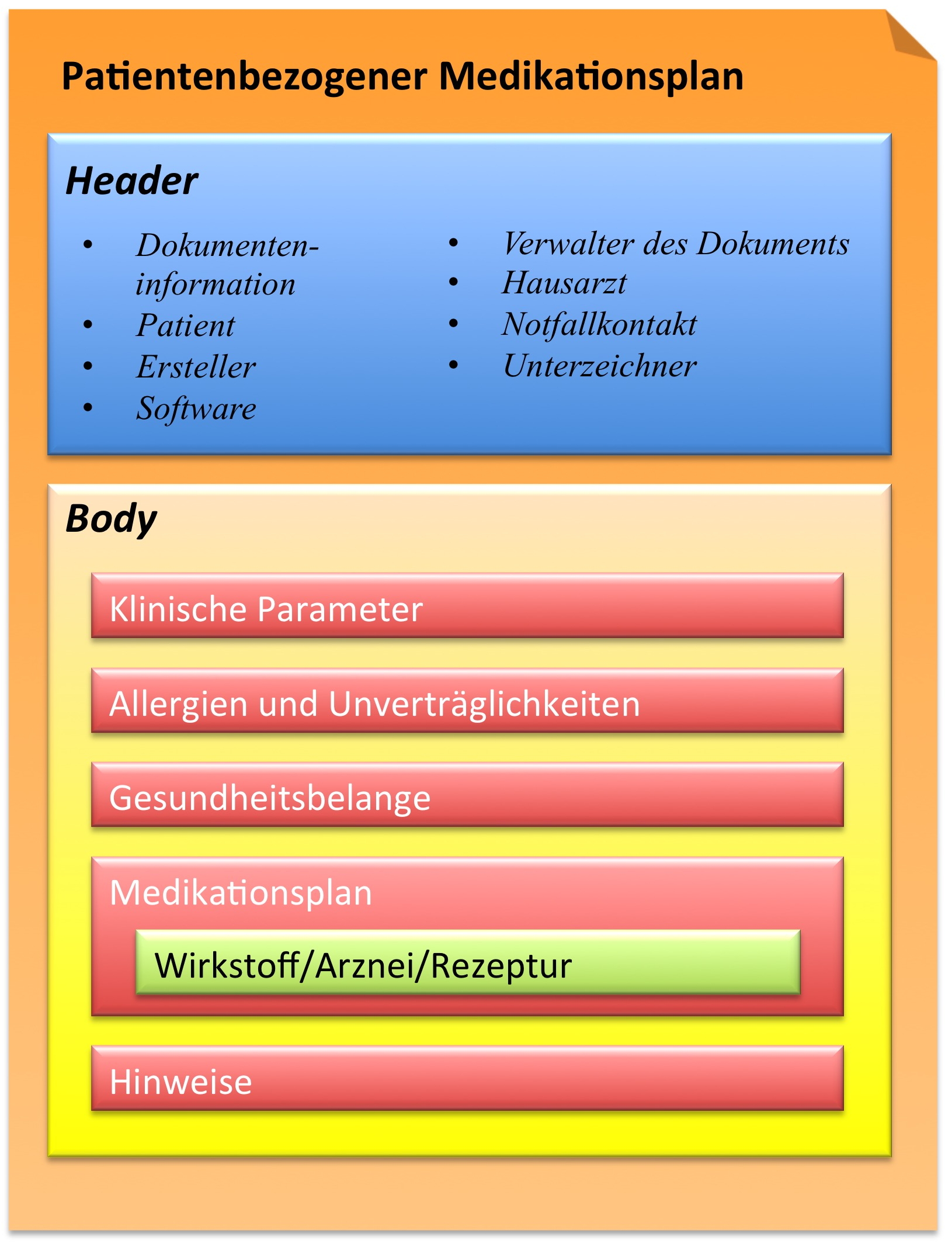
[Abbildung 3] Übersicht CDA Header und Body
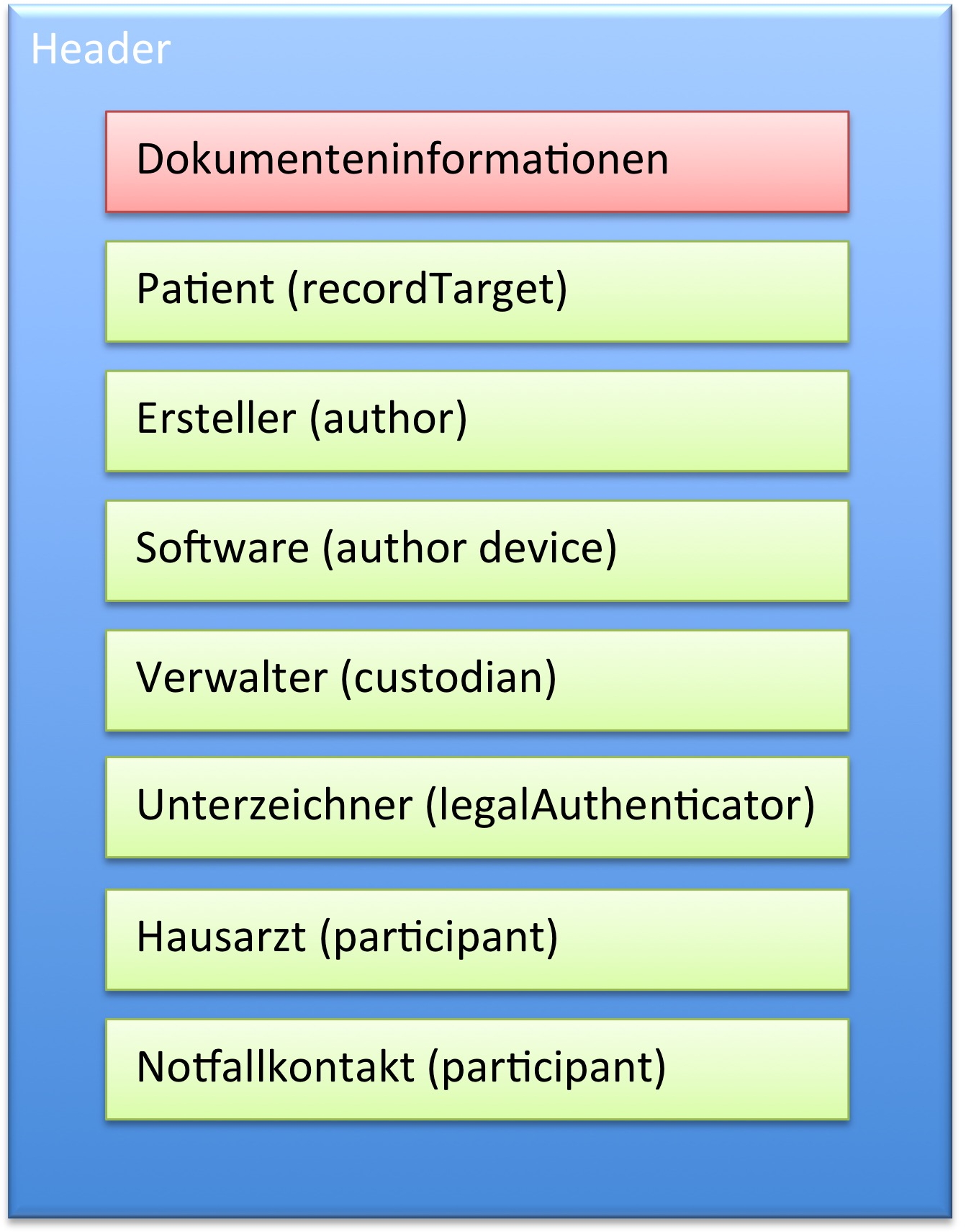
Im Header sind die üblichen und geforderten Angaben
- zum Dokument selbst mit Identifikation, Version, Sprache des Dokuments etc.
- dem Patienten
- dem Ersteller des Plans (Autor)
- der Organisation die das Dokument verwaltet sowie
- mögliche Angaben zur verwendeten Software (Autor)
- mögliche Angaben zum vor dem Gesetz verantwortlichen Unterzeichner (legalAuthenticator) bzw. Unterzeichner (authenticator)
- mögliche Angaben zum Hausarzt
- mögliche Angaben zu Notfallkontakten.
[Abbildung 4] Übersicht CDA Header
Im Body sind fünf Sections anzutreffen:
- Klinische Parameter
- Allergien und Unverträglichkeiten
- Gesundheitsbelange
- Medikationsplan
- Wichtige Angaben/Hinweise
Klinische Parameter
Hier können Klinische Parameter wie Körpergewicht und Kreatinin angegeben werden. Die Section ist ergänzt durch optionale Entries, die die entsprechenden Parameter kodiert wiedergeben.
[Abbildung 5] Übersicht CDA Body Section "Klinische Parameter"
Allergien und Unverträglichkeiten
Hier können Allergien und Unverträglichkeiten aufgeführt werden. Die Section ist ergänzt durch optionale Entries, die die entsprechenden Parameter kodiert wiedergeben.
[Abbildung 6] Übersicht CDA Body Section "Allergien und Unverträglichkeiten"
Gesundheitsbelange
Hier erfolgt eine Beschreibung über einen Gesundheitszustand oder -prozess, der möglicherweise Aufmerksamkeit, Intervention oder Management erfordern könnte. "Gesundheitsbelange" (engl. Health Concern) beschreiben einen Gesundheitszustand oder -prozess, der bedeutsam oder wichtig für den Patienten, die Familie des Patienten oder den behandelnden Arzt/Gesundheitsdienstleister ist oder Anlass zur Besorgnis liefert. In diesem Falle fokussiert sich die Angabe auf eine mögliche Schwangerschaft bzw. Stillzeit.
Die Section ist ergänzt durch optionale Entries (Schwangerschaft, Stillzeit), die die entsprechenden Parameter kodiert wiedergeben.
[Abbildung 7] Übersicht CDA Body Section "Gesundheitsbelange"
Medikationsplan
Die Angaben zum Medikationsplan selbst (typischerweise in Tabellenform wiedergegeben) sind in dieser Section unterzubringen. Sie umfasst die aktuelle Medikation des Patienten, kann aber auch Hinweise zu abgesetzten oder historischen Medikamenten enthalten. Entries zur Medikation und dem Medikament (Arzneimittel/Wirkstoff/Rezeptur) und dem Dosierschema, die die entsprechenden Parameter kodiert wiedergeben, ergänzen die Section. Im Entry sind gleichermaßen Angaben zur Informationsquelle (Informant) bzw. zum Autor der Medikation möglich, zudem sind Referenzen zu Verordnungen bzw. Abgaben des Medikaments möglich (Bezug mittels Identifikatoren).
[Abbildung 8] Übersicht CDA Body Section "Medikationsplan"
Wichtige Angaben
Hier können Abschließende wichtige Angaben / Hinweise (nur als Text) wiedergegeben werden. Diese Section umfasst keine Entries.
[Abbildung 9] Übersicht CDA Body Section "Wichtige Angaben"
Verwendung von Templates
Wie aus den vorhergehenden Erläuterungen ersichtlich ist, setzt sich ein Dokument aus verschiedenen Komponenten zusammen, die flexibel miteinander kombiniert werden können. Für ein Zusammensetzen der Einzelteile auf den unterschiedlichen Ebenen gibt es detaillierte „Baupläne“, die in CDA auch Templates – oder auch Schablonen oder Muster – genannt werden.
Templates sind vordefinierte und allgemein nutzbare Vorlagen, die Strukturen von Dokumenten, Dokumentteilen oder Datenelementen vorgeben.
In diesem Leitfaden werden vier Typen von CDA-Templates verwendet:
- Document Level Templates
- Header Level Templates
- Section Level Templates (Abschnitte)
- Entry Level Templates (kodierte Information, CDA-Entries)
Im Folgenden werden die CDA-Templates beschrieben, die im Rahmen dieses Leitfadens definiert sind bzw. genutzt werden.
Weitere Hinweise zum Aufbau der Template-Beschreibungen hier und in ART-DECOR® finden sich bei der Dokumentation[24]
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Terminologien
Value Sets
Folgende Value Sets werden genutzt.
- AdministrativeGender (HL7) 2.16.840.1.113883.1.11.1
- ParticipationFunction 2.16.840.1.113883.1.11.10267
- DispensableDrugForm (HL7) 2.16.840.1.113883.1.11.14412
- RouteOfAdministration (HL7) 2.16.840.1.113883.1.11.14581
- Basic Confidentiality Kind (HL7) 2.16.840.1.113883.1.11.16926
- ParticipationSignature (HL7) 2.16.840.1.113883.1.11.10282
- RoleClassMutualRelationship (HL7) 2.16.840.1.113883.1.11.19316
- PersonalRelationshipRoleType (HL7) 2.16.840.1.113883.1.11.19563
- Einnahmezeitpunkte 2014-11-19 Final 2.16.840.1.113883.2.60.4.11.20
- AKdÄ Darreichungsform 2013-12-15 Final 2.16.840.1.113883.2.60.4.11.2
- AKdÄ Dosiereinheit 2013-12-15 Final 2.16.840.1.113883.2.60.4.11.4
- epSOSDoseForm 2013-06-03 Final 1.3.6.1.4.1.12559.11.10.1.3.1.42.2
- epSOSRouteofAdministration 2013-06-03 Final 1.3.6.1.4.1.12559.11.10.1.3.1.42.12
Kodesysteme
Folgende Kodesysteme werden genutzt.
- LOINC (2.16.840.1.113883.6.1)
- Snomed (2.16.840.1.113883.6.96)
- diverse Kodesysteme von HL7
- Pharmazentralnummern PZN
- ATC in der jeweils gültigen amtlichen Fassung
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Appendix (nicht normativ)
Kritische Anmerkungen zur Spezifikation des Medikationsplans der AkdÄ in der alten Fassung (vor 2016)
Die „Bundeseinheitlicher Medikationsplan“[7] genannte Spezifikation in der Fassung vor 2016 besteht im Grunde aus zwei Teilen: den Dokumentation der medizinisch-inhaltlichen Vorgaben und der technischen Beschreibung eines Formates zur Unterbringung der Informationen auf einem Barcode.
Der erste Teil stellt die gut erfasste, konsentierte und dokumentierte nationale Vorgabe dar. Diese Angaben sollen als inhaltlicher Ausgangspunkt für einen einheitlichen Medikationsplan angesehen werden und sind – wie bereits erwähnt – die Grundlage für die hier vorliegende Spezifikation des Patientenbezogenen Medikationsplans.
Die technische Beschreibung in der Fassung vor 2016 ist die Definition eines proprietären Formats, das nur hierfür zusammengestellt wurde. Nach Analysen (unter anderem in [25]) offenbaren sich jedoch eine Reihe von Problemen des Formats:
- es weist technische und inhaltliche Fehler auf, die zugrundeliegende Grammatik ist in der vorliegenden Definition problematisch (siehe auch [25])
- es ist nicht spezifisch genug, was zu Missinterpretation der Softwarehersteller führt.
- es stellt keine moderne Schnittstellenbeschreibung dar und unterlag keiner formalen Konsentierung, z.B. nach ISO/TR 28380-1:2014[26]
- es nutzt keine gängigen IT-Standards
- es nutzt kaum offizielle Terminologien, die meisten Kode-Listen sind proprietär; in der jüngsten vorliegenden Fassung sind Kodes selbst überwiegend verbannt, was zu weiteren Problemen führen kann
- als proprietäres Format kann es nur in diesem Kontext verwendet werden, eine Interoperabilität mit anderen Anwendungen (selbst AMTS-Anwendungen zum Beispiel) ist schwer herzustellen
- es ist abzusehen, dass die Implementierung dieses Formats vermeidbare Kosten verursacht.
Hinzu kommen noch grundsätzlich orientierte Probleme, die bei der Umsetzung von proprietären Formaten zu erwarten sind:
- Um die Daten aus einer Anwendung in die beschriebene Form zu bringen (Serialisierung) ist ein spezieller Generator nötig. Diesen muss jedes Softwareunternehmen entweder selber schreiben oder er wird von Ihrer Seite zur Verfügung gestellt. Es ist unbekannt, ob ein solcher Generator für die Serialisierung frei verfügbar ist.
- Um die Daten, die in dieser Syntax eingebettet sind, wieder auslesen zu können, z. B. um sie weiterzuverwenden, muss von jedem Anbieter von Software ein spezieller und robuster Parser programmiert bzw. eingesetzt werden. Der Parser verwandelt die serialisierte Form wieder in Datenobjekte der lesenden Anwendung um, damit diese weiterverwendet oder geändert und in eine neue Version des Plans für den Patienten umgesetzt werden können. Es ist unbekannt, ob ein solcher Parser frei verfügbar ist. Parser müssen robust sein, weil man davon ausgehen muss, dass nicht alle Serialisierungen korrekt sind und man eine Chance haben muss, dies auch zu entdecken.
- Für die Sicherstellung, ob ein Datensatz in dieser Syntax formal korrekt serialisiert ist braucht man einen Validator der die Regeln der Syntax überprüft. Dazu ist es auch nötig, die zugrundeliegende Grammatik formal zu beschreiben, zum Beispiel in der üblichen Backus-Naur-Form. Ohne Validator, der auch Bestandteil des Parsers sein kann, ist eine Garantie darauf, dass die Daten korrekt wiedergegeben und wiederverwendet werden können nicht gegeben. Eine Zertifizierung ist ohne Validator äußerst schwierig.
- Die Syntax mischt zuweilen Anweisungen zum Druck für die Papierfassung mit den eigentlichen Daten. Ein Parser muss diese Druckinstruktionen aus der Serialisierung holen, denn diese können sich bei veränderten Daten natürlich auch ändern. Üblich ist Struktur und Präsentation zu trennen.
Aus diesen Gründen wird auch im NRW-Projekt vom technischen Teil abgesehen und das dort entwickelte Ultrakurzformat XML verwendet.
Des Weiteren muss als Kritikpunkt angeführt werden, dass das Wiedergabeformat des Medikationsplans der AkdÄ eine Insellösung darstellt, die in keiner Weise interoperabel zu anderen Anforderungen ist. So stellt die Wiederverwendung von Medikationsdaten – selbst in domänenzugehörigen Anwendungen zur Arzneimitteltherapiesicherheit AMTS, erst recht in domänenabgelegenen Anwendungen wie zum Beispiel im Rahmen eines Ärztlichen Entlassbriefs oder von der Dokumentation von Notfalldaten – eine unbillige Hürde dar.
Anmerkungen zur Spezifikation des Medikationsplans laut §291a bzw. nach § 31a in der Fassung ab April 2016
Inzwischen wurde die technische Repräsentierung der Information im Barcode derart geändert, so dass sie dem (leicht angepassten) Ultrakurzformat[20] entspricht.
Aspekte zur Mehrsprachigkeit
In Deutschland leben laut einem Bericht der Bundesregierung[27] ca. 20% Ausländer oder Deutsche mit Migrationshintergrund. Um sprachlichen Problemen abzuhelfen, setzen daher einige Leistungserbringer mit ihren Medikationsplänen im Routinebetrieb auf mehrsprachige Ausdrucke, vor allem in Bezug auf die Patientenhinweise und –instruktionen (vgl. [8]).
Voraussetzung für eine korrekte Zuordnung und Interoperabilität der einzelnen Angaben in einem Medikationsplan ist eine weit gehende Kodierung der Angaben, Hinweise und Instruktionen. Mit der Version vom 18. Dezember 2014 hat allerdings die Koordinierungsgruppe der Arzneimittelkommission der deutschen Ärzteschaft beschlossen, gerade diese Kodierungen (zunächst) aus der Spezifikation zu streichen.
Die Hersteller von Software, insbesondere Arzneimitteldatenbank-Anbieter, haben bereits Listen solcher Angaben, Hinweise und Instruktionen – teilweise auch mehrsprachig – und könnten somit wertvolle Beiträge bei der Aufstellung solcher in Deutschland einheitlicher Kataloge (Listen) leisten. Wenn diese Listenelemente entsprechend kodiert und einheitlich zur Verfügung stehen würden, käme man optimalen Möglichkeiten von mehrsprachigen Medikationsplänen ein großes Stück näher.
Lizenzen
HL7
Health Level Seven® International (HL7) standards and other "Material," as defined below, and Material acquired through any channel (including through any HL7 Affiliate) are governed by the terms of this HL7 policy. All such Material are copyrighted by HL7 and protected by the Copyright Law of the United States and copyright provisions of various international treaties. See HL7 Policy governing the use of HL7® international standards and other intellectual property at http://www.hl7.org/legal/ippolicy.cfm
Logical Observation Identifiers Names and Codes LOINC
This material contains content from LOINC® (http://loinc.org). The LOINC table, LOINC codes, and LOINC panels and forms file are copyright © 1995-2014, Regenstrief Institute, Inc. and the Logical Observation Identifiers Names and Codes (LOINC) Committee and available at no cost under the license at http://loinc.org/terms-of-use.
SNOMED Clinical Terms® (SNOMED CT®)
This material includes SNOMED Clinical Terms® (SNOMED CT®) which may not be used without permission of the International Health Terminology Standards Development Organisation (IHTSDO). All rights reserved. SNOMED CT®, was originally created by The College of American Pathologists. “SNOMED” and “SNOMED CT” are registered trademarks of the IHTSDO.
Amtlicher ATC-Index mit DDD-Angaben
Das Wissenschaftliche Institut der AOK (WIdO) erteilte am 1. Dezember 2014 die Genehmigung zur unentgeltlichen Nutzung des amtlichen ATC-Index mit DDD-Angaben, der jeweils zum Stichtag 1. Januar eines Jahres in Kraft tritt und auf der Homepage http://www.wido.de/amtl_atc-code.html veröffentlicht wird, zur Verwendung in Projekten zum Medikationsplan.
Dabei ist Folgendes zu beachten: Es ist untersagt, den amtlichen ATC-Index mit DDD-Angaben darüber hinausgehend – auch nur teilweise –für andere Zwecke, insbesondere für kommerzielle Zwecke zu nutzen, Änderungen oder Manipulationen im amtlichen ATC-Index mit DDD-Angaben vorzunehmen. Der Nutzer ist verpflichtet, bei wissenschaftlichen Veröffentlichungen und insbesondere bei wissenschaftlich genutzten abgeleiteten Werken in digitaler Form an prominenter Stelle folgenden Hinweis zu platzieren „Datenquelle des amtlichen ATC-Index mit DDD-Angaben: GKV-Arzneimittelindex im Wissenschaftlichen Institut der AOK (WIdO), AOK Bundesverband GbR Stand „Datum““. Der Nutzer verpflichtet sich dem Wissenschaftlichen Institut der AOK (WIdO) etwaige Publikationen, die auf der Anwendung der Daten des GKV-Arzneimittelindex basieren, dem WIdO unverzüglich nach der Veröffentlichung in zwei Exemplaren unentgeltlich zur Verfügung zu stellen und gegebenenfalls eine Lizenz zur kostenfreien Nutzung der Datenbank zur Verfügung zu stellen.
Pharmazentralnummern
Informationsstelle für Arzneispezialitäten (IFA)
Projektträger und -kontributoren
Referenzen
Verweise
- ↑ Sondergutachten des Sachverständigenrat zur Begutachtung der Entwicklung im Gesundheitswesen: Wettbewerb an der Schnittstelle zwischen ambulanter und stationärer Gesundheitsversorgung, 2012 http://www.svr-gesundheit.de/index.php?id=378, zuletzt besucht 2015-01-04
- ↑ Dr. med. Amin-Farid Aly: Der einheitliche patientenbezogene Medikationsplan. Vortrag Session Gesundheitstelematik – conhIT 2014, http://www.akdae.de/Fortbildung/Vortraege/Weitere/2014-conhit.pdf, zuletzt besucht am 5. Januar 2015
- ↑ Executive summary of the American Society of Health System Pharmacists (ASHP) and ASHP Research and Education Foundation Continuity of Care in Medication Use Summit. Am J Health Syst Pharm. Bethesda, Maryland June 5–6, 2007, Am J Health-Syst Pharm. 2008; 65:e3-9
- ↑ The Patient Medication List: Can We Get Patients More Involved in Their Medical Care? Sung Y. Chae, MD, Mark H. Chae, PhD, Nicole Isaacson, PhD, LSW and Tarika S. James, MD. J Am Board Fam Med November-December 2009 vol. 22 no. 6 677-685
- ↑ Medication Therapy Management in Pharmacy Practice: Core Elements of an MTM Service Model, Version 2.0, March 2008. A joint initiative of the American Pharmacists Association and the National Association of Chain Drug Stores Foundation
- ↑ M. Staemmler: Der patientenbezogene Medikationsplan: Was leistet er im Vergleich mit bestehenden Lösungen? GMDS 2014. 59. Jahrestagung der Deutschen Gesellschaft für Medizinische Informatik, Biometrie und Epidemiologie e.V. (GMDS). Göttingen, 07.-10.09.2014. Düsseldorf: German Medical Science GMS Publishing House; 2014. DocAbstr. 338, http://www.egms.de/static/de/meetings/gmds2014/14gmds010.shtml
- ↑ 7,0 7,1 7,2 7,3 Medikationsplan der Arzneimittelkommission der deutschen Ärzteschaft (AkdÄ) Version 2.0 (15. Dezember 2013) und der aktualisierten Version 2.0 (18. Dezember 2014), http://www.akdae.de/AMTS/Medikationsplan/index.html, zuletzt besucht am 5. Januar 2015
- ↑ 8,0 8,1 Medikationsplan am Universitätsklinikum Heidelberg, z. B. http://www.klinikum.uni-heidelberg.de/ShowSingleNews.176.0.html?&no_cache=1&tx_ttnews%5Btt_news%5D=6754, http://www.das-apotheker-forum.de/de/pharmazie/news/7536-Neuer_Medikationsplan_erleichtert_Einnahme/
- ↑ Deutsche Krankenhausgesellschaft (DKG), http://www.dkgev.de
- ↑ Medikationsplan Projektseite des Interoperabilitätsforums, http://wiki.hl7.de/index.php/Medikationsplan_(Projekt)
- ↑ IHE Pharmacy Profiles, http://www.ihe.net/Pharmacy
- ↑ IHE Template "Medications" 1.3.6.1.4.1.19376.1.5.3.1.4.7, http://wiki.ihe.net/index.php?title=1.3.6.1.4.1.19376.1.5.3.1.4.7
- ↑ ELGA Implementierungsleitfaden: HL7 Implementation Guide for CDA® R2: e-Medikation, http://www.elga.gv.at/index.php?id=28
- ↑ ART-DECOR Spezifikation zum ELGA Implementierungsleitfaden: HL7 Implementation Guide for CDA® R2: e-Medikation http://art-decor.org/art-decor/decor-project--elga-
- ↑ epSOS-Projekt, http://www.epsos.eu
- ↑ ART-DECOR Spezifikation zum epSOS-Projekt, http://decor.nictiz.nl/art-decor/decor-project--epsos-
- ↑ Arztbrief des VHitG (jetzt bvitg), http://www.bvitg.de/arztbrief.html
- ↑ eArztbrief 2014, http://wiki.hl7.de/index.php/IG:Arztbrief_2014
- ↑ CDA-CH-SMTL shared medication treatement list, Guide d’implémentation pour la SMTL V1.0, Entwurf 2014
- ↑ 20,0 20,1 Addendum zum Implementierungsleitfaden Patientenbezogener Medikationsplan: Ultrakurzformat für kapazitätslimitierte Datenträger (UKFPMP) http://wiki.hl7.de/index.php?title=IG:Ultrakurzformat_Patientenbezogener_Medikationsplan
- ↑ Erstellung von XML-Signaturen für Dokumente nach Clinical Documents Architecture – R2 (Elektronische Signatur von Arztbriefen). Spezifikation der Bundesärztekammer, Ärztekammer Nordrhein, Ärztekammer Westfalen-Lippe. Version 1.4 vom 20. Mai 2008
- ↑ Telematikinfrastruktur und Telemedizin in Deutschland – Bilanz und Ausblick. Mathias Redders, Referatsleiter Telematik im Gesundheitswesen, MGEPA NRW. Beitrag 1. Nationaler Fachkongress Telemedizin – 4. November 2010
- ↑ ART-DECOR Spezifikation zum CDA-basierten Patientenbezogenen Medikationsplan, http://art-decor.org/art-decor/decor-project--pmp-
- ↑ How to read ART-DECOR Definitions https://art-decor.org/mediawiki/index.php?title=How_to_read_ART-DECOR_Definitions.
- ↑ 25,0 25,1 F. Oemig: AKdÄ-Medikationsplan - Felder aus dem AKdÄ-Medikationsplan, Grammatik und Probleme, http://wiki.hl7.de/index.php/IG:AKdÄ-Medikationsplan#Anhang
- ↑ ISO/TR 28380-1:2014 Health informatics -- IHE global standards adoption -- Part 1: Process, http://www.iso.org/iso/home/store/catalogue_tc/catalogue_detail.htm?csnumber=63383
- ↑ 10. Bericht der Beauftragten der Bundesregierung für Migration, Flüchtlinge und Integration über die Lage der Ausländerinnen und Ausländer in Deutschland (Oktober 2014)
Abbildungsverzeichnis
- ↑ Übersicht zur funktionalen Beschreibung des Patientenbezogenen Medikationsplan
- ↑ Zusammenhang zwischen funktionaler Beschreibung und technischer Spezifikation
- ↑ Übersicht CDA Header und Body
- ↑ Übersicht CDA Header
- ↑ Übersicht CDA Body Section "Klinische Parameter"
- ↑ Übersicht CDA Body Section "Allergien und Unverträglichkeiten"
- ↑ Übersicht CDA Body Section "Gesundheitsbelange"
- ↑ Übersicht CDA Body Section "Medikationsplan"
- ↑ Übersicht CDA Body Section "Wichtige Angaben"