AKdÄ-Medikationsplan auf der Basis von CDA R2
|
|
Dieses Dokument gibt wieder:
Implementierungsleitfaden AKdÄ-Medikationsplan auf der Basis von CDA R2 (01). Die Teilmaterialien gehören der Kategorie cdampl an. |
HL7 Clinical Document Architecture Release 2
für das deutsche Gesundheitswesen
| Abstimmungsdokument | |||
|---|---|---|---|
| Version | Datum | Status | Realm |
| 01 | 01.07.2013 | zur Kommentierung | |
| noch kein download verfügbar | |||
| Kontributoren | ||
|---|---|---|
| Agfa HealthCare GmbH | Bonn | |
| 100px | Siemens AG Healthcare Sector | Erlangen |
| 100px | Tieto Deutschland GmbH | Köln |
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Inhaltsverzeichnis
- 1 Einleitung
- 2 Umsetzungsmöglichkeiten
- 3 CDA-Header
- 4 CDA-Body
- 5 CDA-Beispiel
- 6 Anhang
- 7 offene Punkte
- 8 Referenzen
Einleitung
Die Arzneimittelkommission der deutschen Ärzteschaft (AKdÄ) hat zusammen mit der AG AMTS des bvitg eine Spezifikation für einen Medikationsplan erstellt (www.akdae.de/AMTS/Massnahmen/docs/Medikationsplan.pdf). Diese Spezifikation dient primär für einen Ausdruck der aktuellen Medikation, um diese dem Patienetn mitzugeben. Über einen Barcode ist auch ein Austausch der aktuellen Medikationsdaten zwischen APIS und KIS möglich. Hier stand eine möglichst einfache Umsetzbarkeit sowie ein Datenaustausch über den Barcode im Vordergrund. Die proprietäre Spezifikation wurde und wird mit der Längenbeschränkung des Barcodecarriers begründet.
Diese Initialfassung eines Implementierungsleitfadens demonstriert, dass diese Spezifikation auch mit CDA sehr leicht umsetzbar ist (vgl. Layoutbeispiele nachfolgend).
Alternativen
Die im Interoperabilitätsforum durchgeführten Arbeiten haben eindruckscoll bewiesen, dass die inhaltlichen Vorgaben des BMP verlustfrei auf Basis von Standards realisiert werden können. Alle Anforderungen sind über den patientenbezogenen Medikationsplan mit Hilfe von XML umsetzbar. Die Längenbeschränkung des Barcode-Carriers führen jedoch dazu, dass ein vollständiges CDA-Dokument nicht direkt darin enthalten sein kann. Durch eine bijektive Transformation ist jedoch eine verkürzte und vereinfachte XML-Darstellung möglich. Hierdurch werden zum einen XML-Basis-Tools nutzbar, für die es umfangreiche Bibliotheken gibt, zum anderen hat jeder Hersteller die freie Wahl, ob er die verkürzte XML-Fassung oder ein korrekte CDA-Dokument nutzen möchte. Darüber hinaus ist eine Validierung der Inhalte möglich.
Die Spezifikation ist als PMP fertig erstellt, abgestimmt, verfügbar und in NRW erfolgreich im Test.
Damit ist unerklärbar, warum an der nachteiligen, ineffizenten, mehrdeutigen, proprietären und somit Zusatzaufwände produzierenden technischen Spezifkation festgehalten wird.
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
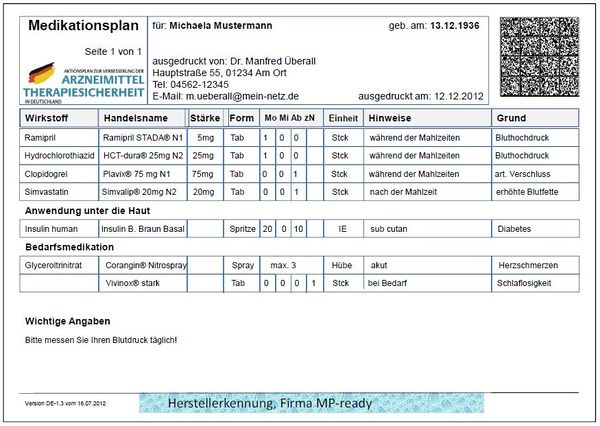
Original-Layout
Nachfolgend das Layout als Auszug aus der Originalspezifikation:
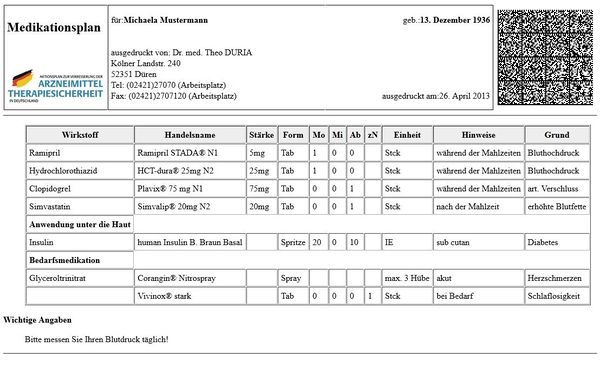
CDA-Layout
Nun das Layout, das durch ein Stylesheet aufbereitet wurde. Das Datamatrix-Barcode wurde dabei aus dem Observation-Entry gerendert:
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Umsetzungsmöglichkeiten
Der Medikationsplan kann auf unterschiedliche Weise mit jeweils individuellen Vor- und Nachteilen umgesetzt werden. Diese werden nachfolgend kurz aufgelistet.
1. PDF in CDA
Die einfachste Möglichkeit ist der Ausdruck gemäß AKdÄ-Spezifikation mit Einbettung des daraus entstehenden PDFs in einem CDA-Dokument. Damit wäre aber keine Wiederverwendbarkeit gegeben, die auch zu einer neuen Version des Dokuments führt. Dieshalb wird diese Version hier wieder verworfen.
2. einfaches CDA mit 2 Abschnitten und simplen Entry
Diese Variante ist nicht kompliziert und entspricht am ehesten einer direkten Umsetzung der Originalspezifikation. Hierbei können die Daten ebenfalls geparst und auch als Datamatrixcode ausgedruckt werden. Das ist die hier verfolgte einfache Variante.
3. CDA mit Modell auf Entrylevel
Hier werden die Daten in einzelnen Entries repräsentiert. Damit wird jede Information einzeln beschrieben und auch wiederverwendbar. Jedoch wird die Spezifikation insgesamt deutlich umfangreicher und komplizierter, der Barcode muss dann erst errechnet werden. Hier sollten dann Sektions und Entries erarbeitet werden, die auch in anderen Dokumenttypen wiederverwendet werden können.
Diese Variante wird hier auf Basis des Addendums Medikation beschrieben.
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
CDA-Header
Der Header besteht - neben den Grundinformationen aus dem Arztbrief - aus folgenden Elementen:
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Patient (recordTarget - generisch)
| Id | 1.2.276.0.76.10.2001 | Gültigkeit | 2013‑07‑10 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | HeaderRecordTarget | Bezeichnung | CDA recordTarget | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Offen (auch andere als die definierten Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Spezialisierung: Template 2.16.840.1.113883.10.12.101 CDA recordTarget (DYNAMIC) ref ad1bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Verwaltende Organisation (custodian - generisch)
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Autor (author - generisch)
| Id | 1.2.276.0.76.10.2002 | Gültigkeit | 2013‑07‑10 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | HeaderAuthor | Bezeichnung | CDA author | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Die Autor-Relation gibt den Urheber der Dokumentation und den Zeitpunkt der Autorenschaft wieder. Dies sind in der Regel Personen (Gesundheitsdienstleister) oder auch Geräte, die Daten erzeugen. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Offen (auch andere als die definierten Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Spezialisierung: Template 2.16.840.1.113883.10.12.102 CDA author (DYNAMIC) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Unterzeichner gesetzlich verantwortlich (legalAuthenticator - generisch)
| Id | 1.2.276.0.76.10.2020 | Gültigkeit | 2014‑08‑25 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | HeaderLegalAuthenticator | Bezeichnung | CDA legalAuthenticator | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Vor dem Gesetz verantwortliche Unterzeichner des Dokumentes | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Header Level Template | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Offen (auch andere als die definierten Elemente sind erlaubt) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Benutzt |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Spezialisierung: Template 2.16.840.1.113883.10.12.106 CDA legalAuthenticator (2005‑09‑07) ref ad1bbr- | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beispiel |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
CDA-Body
Der Body besteht im wesentlichen aus zwei Teilen:
- der Medikation
- weiterer wichtiger Hinweise
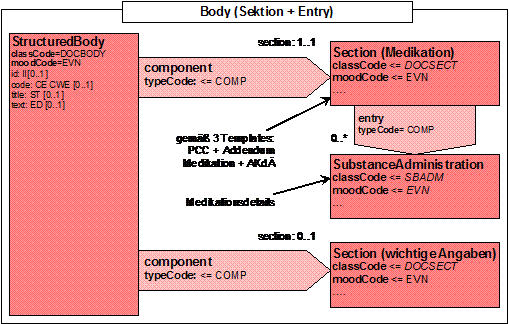
Dies wird durch nachfolgendes Schaubild verdeutlicht:
Die Abschnitte und die dazugehörigen Details werden dabei gemäß mehrerer Vorgaben aufbereitet. So gehorcht der Abschnitt Medikation sowohl dem Addendum Medikation des VHitG-Arztbriefes als auch der Vorgabe zur textuellen Darstellung der Medikation in Form einer Tabelle.
Dazu kommt dann noch der zweite optionale Abschnitt mit weiteren wichtigen Angaben.
Die notwendigen Details werden nachfolgend vorgestellt:
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Section: Medikationen
In diesem Leitfaden werden folgende Templates zu Medikations-Informationen unterstützt:
Medikation bei Einweisung (Historie)
| Id | 1.2.276.0.76.10.3029 | Gültigkeit | 2013‑12‑30 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | Admissionmedicationsection | Bezeichnung | Medikation bei Einweisung (Historie) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Erhobene Medikation bei Aufnahme des Patienten. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Offen (auch andere als die definierten Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Spezialisierung: Template 2.16.840.1.113883.10.12.201 CDA Section (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Verabreichte Medikation während des Aufenthalts
| Id | 1.2.276.0.76.10.3030 | Gültigkeit | 2013‑12‑30 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | Medicationduringstaysection | Bezeichnung | Verabreichte Medikation während des Aufenthalts | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Sämtliche verabreichte Medikation während des Aufenthalts | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Offen (auch andere als die definierten Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Spezialisierung: Template 2.16.840.1.113883.10.12.201 CDA Section (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Medikation bei Entlassung
| Id | 1.2.276.0.76.10.3031 | Gültigkeit | 2013‑12‑30 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Status | Versions-Label | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Name | Dischargemedicationsection | Bezeichnung | Medikation bei Entlassung | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beschreibung | Medikation bei Entlassung | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Klassifikation | CDA Section level template | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Offen/Geschlossen | Offen (auch andere als die definierten Elemente sind erlaubt) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Beziehung | Spezialisierung: Template 2.16.840.1.113883.10.12.201 CDA Section (2005‑09‑07) ref ad1bbr- | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Section: Medikation (spezifisch)
| Template-Metadaten | |
| Template-Typ | Section |
| Template ID |
|
| generischeres Template | |
| genutztes Templates | cdaab2:Medikation-Entry_(Template) |
| nutzende Templates | |
| abgeleitete Templates | |
| Schwester-Templates | |
| generelle Beschreibung | Dieser Abschnitt enthält Informationen über die Medikation eines Patienten für den Medikationsplan und schränkt das Template aus cdaab2 in Bezug auf die textuelle Darstellung ein. |
| allg. Erläuterung | |
| Verhältnis zu IHE | neu |
| Ballotierungsstatus | in Arbeit |
| Erweiterbarkeit | offen |
Beschreibung
Dieses Section-Template ist eine Spezialisierung des allgemeinen Medikation Section Templates (auf Basis des Addendums Medikation zum VHitG-Arztbriefes), um eine spezielle Textdarstellung festzulegen. Ansonsten gelten die gleichen Grundlagen.
Einschränkungen auf die textuelle Darstellung
Die Darstellung der Medikation erfolgt direkt im Text - tabellenorientiert. Details dazu finden sich in der AKdÄ-Spezifkation. Die Daten werden in eine Tabelle geschrieben, die die folgenden HTML-Strukturierungselemente nutzt:
- table
- thead
- tbody
- tr
- td
- th
- styleCode (für Fettschrift)
Attribute
| Lvl | RIM | Element | DT | Kard. | Opt. | Beschreibung |
|---|---|---|---|---|---|---|
| 1 | act | Section | 1..1 | M | ||
| 2 | act | Title | ST | 1..1 | F | Medikationsplan |
| 2 | act | Text | 1..1 | M | Constraints s.u. | |
| 3 | act | table | 1..1 | M | Darstellung als Tabelle | |
| 4 | act | @border | 1..1 | M | fix: "1" | |
| 3 | act | thead | 1..1 | M | Tabellenkopf | |
| 4 | act | tr | 1..1 | M | Tabellenzeile im Kopf | |
| 5 | act | th | 11..11 | M | jeweils 1 Tabellenzelle für:
| |
| 3 | act | tbody | 1..1 | M | Tabellenrumpf | |
| 4 | act | tr | 1..* | M | Tabellenzeilen im Rumpf | |
| 5 | act | th | 11..11 | M | jeweils 1 Tabellenzelle für die einzelnen Informationen zu:
Wenn diese Information nicht vorhanden ist, so ist doch eine leere Zelle anzulegen! |
Constraints
- Vorgaben für die textuelle Darstellung der Medikation als Tabelle.
| Spalte | Beschreibung |
|---|---|
| Wirkstoff | |
| Handelsname | |
| Stärke | Dosis |
| Form | Darreichungsform |
| Mo | Morgens |
| Mi | Mittags |
| Ab | Abends |
| zN | Zur Nacht |
| Einheit | |
| Hinweise | |
| Grund |
Beispiel
| Wirkstoff | Handelsname | Stärke | Form | Mo | Mi | Ab | zN | Einheit | Hinweise | Grund |
|---|---|---|---|---|---|---|---|---|---|---|
| Ramipril | Ramipril STADA® N1 | 5mg | Tab | 1 | 0 | 0 | Stck | während der Mahlzeiten | Bluthochdruck |
<section>
<templateID root="" extension="" />
<title>Medikationsplan</title>
<text>
<table border="1">
<thead>
<tr>
<th>Wirkstoff</th>
<th>Handelsname</th>
<th>Stärke</th>
<th>Form</th>
<th>Mo</th>
<th>Mi</th>
<th>Ab</th>
<th>zN</th>
<th>Einheit</th>
<th>Hinweise</th>
<th>Grund</th>
</tr>
</thead>
<tbody>
<tr>
<td>Ramipril</td>
<td>Ramipril STADA® N1</td>
<td>5mg </td>
<td>Tab</td>
<td>1</td><td> 0</td><td>0</td><td></td>
<td>Stck</td>
<td> während der Mahlzeiten </td>
<td>Bluthochdruck</td>
</tr>
</tbody>
</table>
</text>
</section>
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Entry: Medikation
| Template-Metadaten | |
| Template-Typ | Entry |
| Template ID | |
| generischeres Template | |
| genutztes Templates |
|
| nutzende Templates | cdaab2:Medikation-Section_(Template), Cdampl:Medikation-Section_(Template) |
| abgeleitete Templates | |
| Schwester-Templates | |
| generelle Beschreibung | Dieser Abschnitt enthält Informationen über die Medikation eines Patienten in kodierter Form.
Dies ist das Addendum-Medikation des VHitG-Arztbriefes. |
| allg. Erläuterung | |
| Verhältnis zu IHE | dt.Übersetzung oder Ergänzung oder neu |
| Ballotierungsstatus | |
| Erweiterbarkeit | offen |
Beschreibung
Die Klasse SubstanceAdministration sowie weitere Klassen, die dazu in Beziehung stehen, wird genutzt, um Medikationsangaben zu dokumentieren. Die Klasse SubstanceAdministration repräsentiert dabei die Verordnung/Verabreichung eines Medikaments. In dieser Klasse werden vor allem die Zeitangaben zur Einnahme, Dringlichkeit, Verabreichungsinformationen sowie Dosierung angegeben.
Im einfachsten Fall enthält SubstanceAdministration eine Verordnung mit einer Dosierung zu ein oder mehreren Zeiten. Es kann pro Instanz der Klasse genau eine Dosierung angegeben werden. Wechseln Dosierungen über die Zeit, z. B. „morgens 1 Tablette, mittags 2 Tabletten, abends 1 Tablette" etc., dann wird die Klasse wiederholt genannt mit der jeweiligen Dosierung und den zugehörigen Zeiten. Dies wird im Abschnitt „Dosierung/ Zeitangaben" genauer beschrieben.
Zur Klassifikation des Medikaments führt die consumable Beziehung über die Rolle ManufacturedProduct zu einem LabeledDrug, also im Wesentlichen zu einer Handelspackung, oder eine reine Stoffbeschreibung über Material. Über code wird das Medikament klassifiziert. Im Folgenden werden die Attribute der beteiligten Klassen im Detail beschrieben.
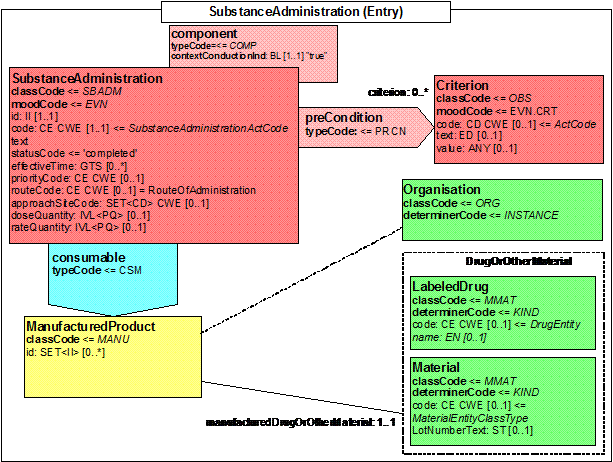
Modell
Abbildung 2: substanceAdministration (cdampl_sbdam.gif)
Attribute
| Lvl | RIM | Element | DT | Kard. | Opt. | Beschreibung |
|---|---|---|---|---|---|---|
| 1 | act | SubstanceAdministration | M | Die Klasse SubstanceAdministration trägt die eigentliche Verordnung/ Verabreichung.
| ||
| 2 | act | @classCode | 1..1 | F | SBADM | |
| 2 | act | @moodCode | M | Mood-Code = EVN oder INT:
Der Mood-Code der hier spezifizierten Verordnung/Verabreichung ist entweder im Falle einer beabsichtigten Verordnung/Verabreichung INT (Intend) oder im Falle tatsächlicher Verordnungen/Verabreichungen EVN (Event). Verordnungen im Sinne eines Rezeptes (request RQO) sind nicht Gegenstand eines Arztbrief CDA Dokuments. | ||
| 2 | act | Id | II | 0..* | O | Verordnungsidentifikation : Es ist empfehlenswert, jeder Verordnung eines Medikaments in einem System eine Identifikation zuzuordnen (II). Damit wird eine gezielte Kommunikation über Verordnungen möglich, zum Beispiel der eindeutige Bezug auf Verordnungen. |
| 2 | act | Code | CD CWE | 0..1 | O | Verordnungsklassifizierung : Mit diesem optionalen Code kann die Verordnung/Verabreichung klassifiziert werden. Folgende Werte sind in diesem Zusammenhang sinnvoll.
Es ist ein Wert aus ActSubstanceAdministrationCode zu übertragen. |
| 2 | act | text | ED | 0..1 | O | Der Hinweistext ist die textliche Repräsentation der Verordnung. Er entspricht dem Text, der in Level 1 / 2 niedergeschrieben ist. |
| 2 | act | statusCode | CS CNE | 0..1 | O | Status der Verabreichung
Fix: Active\|completed Der statusCode zeigt an, ob es sich um eine aktive, momentan laufende (active) oder bereits stattgefundene (completed) Verordnung handelt. |
| 2 | act | effectiveTime | GTS | 0..1 | O | Zeitangaben zur Verabreichung : effectiveTime trägt die Zeitangaben zu den Einnahmezeitpunkten. Zusätzlich kann der Zeitraum von wann bis wann das Medikament eingenommen werden soll bzw. verabreicht worden ist, mit angegeben werden. |
| 2 | act | priorityCode | CE CWE | 0..1 | O | Dringlichkeit <= ActPriority
Hiermit wird optional die Dringlichkeit der Verabreichung angedeutet. Es werden hierfür Werte aus der HL7 Codetabelle ActPriority (OID 2.16.840.1.113883.5.7) verwendet. Die zugelassenen bzw. sinnvollen Werte sind der folgenden Tabelle zu entnehmen. |
| 2 | act | routeCode | CE CWE | 0..1 | O | Zugangs-/Verabreichungsweg des Medikaments <= RouteOfAdministration
Hiermit wird der Verabreichungsweg des Medikaments angedeutet, d.h.auf welchem Wege das Medikament in den Körper gelangt bzw. eingenommen werden soll. Hierfür wird die HL7 Codetabelle RouteOfAdministration (OID 2.16.840.1.113883.5.112) verwendet. Diese Codetabelle ist sehr umfangreich und im Prinzip in zwei Teile geteilt. Zum einen kann der Zugangsweg über die Methode der Verabreichung, zum anderen über den Ort der Verabreichung angedeutet werden. Die folgende Tabelle ist ein Auszug aus der RouteOfAdministration. Sie stellt die wahrscheinlich am häufigsten verwendeten Zugangswege zusammen. |
| 2 | act | doseQuantity | IVL<PQ> | 0..1 | O | Dosierungsangaben: Hier wird die Dosierung angegeben. Dies ist in der Regel die Einzeldosis pro Einnahmezeitpunkt oder ein Intervall von Dosierungen wie zum Beispiel 1-2 Tabletten. |
| 2 | act | maxDoseQuantity | RTO<PQ,PQ> | 0..1 | O | Maximale Dosis pro Zeiteinheit : Über dieses Attribut kann die maximale Dosis pro Zeiteinheit angegeben werden. Der Zähler (Nominator) der Verhältnisangabe trägt demzufolge ein Dosisangabe, der Nenner (Denominator) eine Zeitangabe (Periode). |
| 3 | part | consumable | M | Zur Klassifikation des Medikaments führt die consumable Beziehung von der SubstanceAdministration über die Rolle ManufacturesProduct zu einem LabeledDrug, also im Wesentlichen zu einer Handelspackung. | ||
| 4 | part | @typeCode | F | CSM | ||
| 4 | role | ManufacturedProduct | M | Einzunehmendes Produkt | ||
| 5 | role | @classCode | F | MANU | ||
| 5 | role | id | II | 0..* | M | Identifier |
| 5 | ent | LabeledDrug | O | Einzunehmende Substanz (über Produkt):
Hier wird über code und name das Medikament klassifiziert. Das Medikament muss entweder über den Code oder über den Namen (oder beides) angedeutet werden. | ||
| 5 | ent | Code | CE CWE | 0..1 | O | Klassifizierung des Medikatiomes <= DrugEntity
Mit diesem optionalen Code kann das Medikament klassifiziert werden. Mögliche Codesysteme sind in der folgenden Tabelle aufgeführt. |
| 5 | ent | name | EN.DE | 0..1 | O | Name des Medikaments: Mit dieser optionalen Bezeichnung kann das Medikament näher beschrieben werden. |
| 5 | ent | Material | O | Einzunehmende Arznei (als Stoff) | ||
| 5 | ent | Code | CE CWE | O | Vgl. LabeledDrug.code | |
| 5 | ent | Name | EN.DE | O | Vgl. LabeledDrug.name | |
| 5 | ent | lotNumberText | ST | 0..1 | O | Zusätzlich kann eine Chargennummer lotNumberText in Textform angegeben werden. |
| 3 | rel | preCondition | O | |||
| 3 | rel | @typeCode | 1..1 | F | PRCN | |
| 3 | act | Criterion | ||||
| 4 | act | Text | ED | 0..1 | O | Konditionale Verabreichungen, z. B. "1 Tablette bei Schmerzen" sind in Level 3 in der Klasse Criterion in Textform zu dokumentieren. |
Constraints
- Eines der Elemente LabeledDrug oder Material muss vorhanden sein.
Vokabularien
ActCode (ActSubstanceAdministrationCode)
| ||||||||||||||||||||||||||||||||||||||||||||||||||
ActPriority
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
RouteOfAdministration
OID 2.16.840.1.113883.5.112
| Code | Bezeichnung | Erläuterung |
|---|---|---|
| R | Routine | Routineabhandlung |
| CHEW | Chew, oral | kauen, oral |
| DISSOLVE | Dissolve, oral | auflösen, oral |
| SL | Dissolve, sublingual | auflösen, sublingual |
| DOUCHE | Douche, vaginal | Dusche, vaginal |
| ENEMA | Enema, rectal | Einlauf, rektal |
| GARGLE | Gargle | gurgeln |
| IV | Infusion, intravenous | Infusion, intravenös |
| NASINHL | Inhalation, nasal | Inhalation, nasal |
| NEB | Inhalation, nebulization | Inhalation, vernebelt, nasal |
| NASNEB | Inhalation, nebulization, nasal | Inhalation, vernebelt, oral |
| ORINHL | Inhalation, respiratory | Inhalation, oral |
| GINGINJ | Injection, gingival | Injektion, gingival |
| IARTINJ | Injection, intraarticular | Injektion, intraartikulär |
| IDINJ | Injection, intradermal | Injektion, intradermal, intrakutan |
| IEPIDINJ | Injection, intraepidermal | Injektion, intraepidermal |
| IVESINJ | Injection, intravesicle | Injektion, intravesikulär |
| SQ | Injection, subcutaneous | Injektion, subkutan |
| IAINJ | Injection, intraarterial | Injektion, intraartieriell |
| IM | Injection, intramuscular | Injektion, intramuskulär |
| IVINJ | Injection, intravenous | Injektion, intravenös |
| PR | Insertion, rectal | Einführen, rektal |
| URETHINS | Insertion, urethral | Einführen, urethral |
| VAGINSI | Insertion, vaginal | Einführen, vaginal |
| EFT | Instillation, enteral feeding tube | Einträufeln, Ernährungssonde |
| IOINSTL | Instillation, intraocular | Einträufeln, intraokulär |
| NASALINSTIL | Instillation, nasal | Einträufeln, nasal |
| BLADINSTL | Instillation, urinary catheter | Einträufeln, Ureterkatheter |
| URETHINSTL | instillation, urethral | Einträufeln, urethral |
| IOIRR | Irrigation, intraocular | Ausspülen, intraokulär |
| RECIRR | Irrigation, rectal | Ausspülen, rektal |
| ORRINSE | Rinse, oral | Spülung, oral |
| SUCK | Suck, oromucosal | Lutschen, oromukosal |
| URETHSUP | Suppository, urethral | Suppositorium, urethral |
| PO | Swallow, oral | Schlucken, oral |
| SUBCONJTA | Subconjunctival | Oberflächlich auftragen, subkonjunktival |
| TOPICAL | Topical | Oberflächlich auftragen |
| BUC | Topical application, buccal | Oberflächlich auftragen, Wange |
| GIN | Topical application, gingival | Oberflächlich auftragen, gingival |
| SKIN | Topical application, skin | Oberflächlich auftragen, Haut |
| TRNSDERM | Transdermal | Transdermal |
| TRNSLING | Translingual | Translingual |
Codesysteme für Medikamente
| Codesystem | Bezeichnung | Referenz | OID |
|---|---|---|---|
| ABDAMED | Arzneistoffkennung der ABDA | (bislang ohne OID) | |
| ASK | Arzneimittel-Stoffkatalog (ASK) Nummer der Bezeichnungsverordnung nach Rechtsverordnung §10 Abs. 6 Nr. 1 Satz 2 des Arzneimittelgesetzes (AMG) | [dama] | 1.2.276.0.76.5.308 |
| ATC | atcgm2006 Deutsche Fassung der ATC Codes (DIMDI) 2006 |
[atc, dimdi] | 1.2.276.0.76.5.319 |
| ATC | atcgm2007 Deutsche Fassung der ATC Codes (DIMDI) 2007 |
[atc, dimdi] | 1.2.276.0.76.5.320 |
| ATCWidO | Amtliche Fassung des ATC-Index mit DDD-Angaben für Deutschland im Jahre 2007, erstellt vom Wissenschaftlichen Institut der AOK und DIMDI | (bislang ohne OID) | |
| ATCWHO | atcwho2007 WHO Fassung der ATC Codes 2007 |
(bislang ohne OID) | |
| CAS | Chemical Abstract Service | [cas] | 2.16.840.1.113883.6.61 |
| ID MACS | ID MACS | [idmacs] | 1.2.276.0.76.5.305 |
| PZN | Pharmazentralnummer | 1.2.276.0.76.4.6 |
Beispiel
aus PCC
<substanceAdministration classCode="SBADM" moodCode="INT|EVN">
<templateId root="2.16.840.1.113883.10.20.1.24"/>
<templateId root="1.3.6.1.4.1.19376.1.5.3.1.4.7"/>
<templateId root=""/>
<id root="" extension=""/>
<code code="" codeSystem="" displayName="" codeSystemName=""/>
<text><reference value="#med-1"/></text>
<statusCode code="completed"/>
<effectiveTime xsi:type="IVL_TS">
<low value=""/>
<high value=""/>
</effectiveTime>
<effectiveTime operator="A" xsi:type="TS|PIVL_TS|EIVL_TS|PIVL_PPD_TS|SXPR_TS">
:
</effectiveTime>
<routeCode code="" codeSystem="" displayName="" codeSystemName=""/>
<doseQuantity value="" unit=""/>
<approachSiteCode code="" codeSystem="" displayName="" codeSystemName=""/>
<rateQuantity value="" unit=""/>
<consumable>
:
.
</consumable>
<!-- 0..* entries describing the components -->
<entryRelationship typeCode="COMP" >
<sequenceNumber value=""/>
</entryRelationship>
<!-- An optional entry relationship that indicates the reason for use -->
<entryRelationship typeCode="RSON">
<act classCode="ACT" moodCode="EVN">
<templateId root="1.3.6.1.4.1.19376.1.5.3.1.4.4.1"/>
<id root="" extension=""/>
</act>
</entryRelationship>
<!-- An optional entry relationship that provides prescription activity -->
<entryRelationship typeCode="REFR">
<templateId root="1.3.6.1.4.1.19376.1.5.3.1.4.7.3"/>
:
.
</entryRelationship>
<precondition>
<criterion>
<text><reference value=""></text>
</criterion>
</precondition>
</substanceAdministation>
als einzunehmende Arznei
<entry>
<consumable>
<manufacturedProduct>
<manufacturedMaterial>
...
</manufacturedMaterial>
</manufacturedProduct>
</consumable>
</entry>
als einzunehmende Substanz
<entry>
<consumable>
<manufacturedProduct>
<manufacturedLabeledDrug>
<code code="2499914" codeSystem="1.2.276.0.76.4.6"
codeSystemName="Pharmazentralnummer"
displayName="ESIDRIX Tabl. 50 St"/>
<name>Esidrix Tabletten</name>
</manufacturedLabeledDrug>
</manufacturedProduct>
</consumable>
</entry>
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Sektion: wichtige Angaben
| Template ID | tbd |
| verwendetes Template ID: | |
| abgeleitete Templates | tbd |
| General Description | Dieser Abschnitt enthält wichtige Angaben zum Medikationsplan für einen Patienten. |
| Erweiterbarkeit | offen |
Beschreibung
Die wichtigen Angaben werden direkt im Text ausgedrückt. Eine separate Sektion erlaubt eine Abtrennung und eigene Überschrift.
Modell
Attribute
Beispiel
<section>
<code code="xxxxxx" codeSystem="2.16.840.1.113883.6.1" codeSystemName="LOINC"/>
<title>Wichtige Angaben</title>
<text>
Bitte messen Sie Ihren Blutdruck täglich!
</text>
</section>
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Entry: Medikation (Datamatrix-Barcode)
| Template ID | tbd |
| verwendetes Template ID: |
- |
| abgeleitete Templates | tbd |
| generelle Beschreibung | Dieser Abschnitt enthält Informationen über die Medikation eines Patienten in einer vereinfachten Form, die das direkte Generieren eines Datamatrix-Barcodes zulässt. |
| Erweiterbarkeit | offen |
Beschreibung
Dieses Template ist stark vereinfacht und dient ausschließlich dem Zweck, die Daten bereitzustellen, die zum Ausdruck des Datamatrix-Barcodes gemäß der AKdÄ-Spezifkation notwendig sind.
Modell
Das Entry enthält als Observation die Zeichenfolge, die im Datamatrix-Barcode auszudrucken ist.
 |
Eine detailliertes Modell wäre wünschenswert, erhöht aber die Komplexität. |
Attribute
| Template ID | ????? | |
| General Description | Dieser Abschnitt enthält die Informationen für den Barcode. | |
| LOINC Code | Opt. | Description |
| ???? | O | |
| Lvl | RIM | Name | DT | Kard | Conf | Beschreibung |
|---|---|---|---|---|---|---|
| 6 | act | entry | 0..1 | optional | ||
| 7 | act | @moodCode | 1..1 | M | fix: "EVN" Der Mood-Code der hier spezifizierten Prozeduren ist immer EVN (Event), da es sich immer um statt-gefundene Prozeduren handelt. | |
| 7 | act | code | 1..1 | M | ||
| 7 | act | @code | CD CWE | 1..1 | ||
| 7 | act | statusCode | Statuscode <= completed Der statusCode der hier spezifizierten Prozeduren ist immer completed, da es sich immer um eine abgeschlossene Behandlungsmaßnahme handelt. | |||
| 7 | act | effectiveTime | TS | 1..1 | M | |
| 7 | act | value | ST | 1..1 | M | parsbarer String mit der Medikation. Diese Zeichenkette wird gemäß AKdÄ-Spezifikation aufgebaut. |
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
CDA-Beispiel
<?xml version="1.0" encoding="UTF-8"?>
<?xml-stylesheet type="text/xsl" href="mediplan.xsl"?>
<ClinicalDocument xmlns="urn:hl7-org:v3"
xmlns:sciphox="urn::sciphox-org/sciphox"
xmlns:xsi="http://www.w3.org/2001/XMLSchema-instance"
xsi:schemaLocation="urn:hl7-org:v3 d:/archiv/xml/schemas/20040420/CDA.xsd"
>
<typeId root="2.16.840.1.113883.1.3" extension="POCD_HD000040"/>
<id extension="60878,34593" root="1.2.276.0.58"/>
<code code="????" codeSystem="2.16.840.1.113883.6.1" displayName="Medication Plan"/>
<title>Medikationsplan</title>
<effectiveTime value="20130426"/>
<confidentialityCode code="N" codeSystem="2.16.840.1.113883.5.25"/>
<languageCode code="de" />
<setId extension="D1" root="2.16.840.1.113883.3.933"/>
<versionNumber value="1"/>
<recordTarget>
<!--- Patienten-Daten -->
<patientRole>
<id extension="65" root="2.16.840.1.113883.3.933"/>
<addr>
<streetName>Riedemannweg</streetName>
<houseNumber></houseNumber>
<postalCode>13627</postalCode>
<city>Berlin</city>
</addr>
<patient>
<name>
<given>Michaela</given>
<family>Mustermann</family>
</name>
<administrativeGenderCode code="F" codeSystem="2.16.840.1.113883.5.1"/>
<birthTime value="19361213"/>
</patient>
<providerOrganization>
<telecom use="WP" value="tel:(02421)27070"/>
<telecom use="WP" value="fax:(02421)2707120"/>
<addr>
<streetName>Hauptstraße</streetName>
<houseNumber>55</houseNumber>
<postalCode>01234</postalCode>
<city>Am Ort</city>
</addr>
</providerOrganization>
</patientRole>
</recordTarget>
<author>
<!--- author -->
<time value="20070905"/>
<assignedAuthor>
<id extension="2112345" root="2.16.840.1.113883.3.933"/>
<assignedPerson>
<name>
<prefix>Dr. med.</prefix>
<given>Manfred</given>
<family>Überall</family>
</name>
</assignedPerson>
<representedOrganization>
<name>Praxis Dr. Überall</name>
<telecom use="WP" value="tel:(02421)27070"/>
<telecom use="WP" value="fax:(02421)2707120"/>
<addr>
<streetName>Kölner Landstr.</streetName>
<houseNumber>240</houseNumber>
<postalCode>52351</postalCode>
<city>Düren</city>
</addr>
</representedOrganization>
</assignedAuthor>
</author>
<custodian> <!--- Organisation von der das Dokument stammt -->
<assignedCustodian>
<representedCustodianOrganization>
<id extension="M345" root="1.2.276.0.58"/>
<name>Dr. med. Theo DURIA </name>
<telecom nullFlavor="UNK"/>
<addr>
<streetName>Kölner Landstr.</streetName>
<houseNumber>240</houseNumber>
<postalCode>52351</postalCode>
<city>Düren</city>
</addr>
</representedCustodianOrganization>
</assignedCustodian>
</custodian>
<legalAuthenticator> <!--- legalAuthenticator -->
<time value="20070905"/>
<signatureCode code="S"/>
<assignedEntity>
<id extension="2112345" root="2.16.840.1.113883.3.933"/>
<assignedPerson>
<name>
<prefix>Dr. med.</prefix>
<given>Theo</given>
<family>DURIA</family>
</name>
</assignedPerson>
<representedOrganization>
<name>Dr. med. Theo DURIA </name>
<telecom use="WP" value="tel:(02421)27070"/>
<telecom use="WP" value="fax:(02421)2707120"/>
<addr>
<streetName>Kölner Landstr.</streetName>
<houseNumber>240</houseNumber>
<postalCode>52351</postalCode>
<city>Düren</city>
</addr>
</representedOrganization>
</assignedEntity>
</legalAuthenticator>
<component>
<structuredBody>
<component>
<section>
<code code="13133-3" codeSystem="2.16.840.1.113883.6.1" codeSystemName="LOINC"/>
<text>
<table border="1">
<thead>
<tr>
<th>Wirkstoff</th>
<th>Handelsname</th>
<th>Stärke</th>
<th>Form</th>
<th>Mo</th>
<th>Mi</th>
<th>Ab</th>
<th>zN</th>
<th>Einheit</th>
<th>Hinweise</th>
<th>Grund</th>
</tr>
</thead>
<tbody>
<tr>
<td>Ramipril</td>
<td>Ramipril STADA® N1</td>
<td>5mg </td>
<td>Tab</td>
<td>1</td><td> 0</td><td>0</td><td></td>
<td>Stck</td>
<td> während der Mahlzeiten </td>
<td>Bluthochdruck</td>
</tr>
<tr>
<td>
Hydrochlorothiazid </td>
<td>HCT-dura® 25mg N2 </td>
<td>25mg </td>
<td>Tab</td>
<td> 1</td><td> 0</td><td> 0</td><td></td>
<td> Stck</td><td> während der Mahlzeiten </td>
<td>Bluthochdruck</td>
</tr>
<tr>
<td>Clopidogrel </td><td>Plavix® 75 mg N1 </td>
<td>75mg </td>
<td>Tab</td>
<td>0</td><td> 0</td><td> 1 </td><td></td><td>Stck </td>
<td>während der Mahlzeiten </td>
<td>art. Verschluss</td>
</tr>
<tr>
<td>Simvastatin </td>
<td>Simvalip® 20mg N2 </td>
<td>20mg </td><td>Tab</td>
<td>0</td><td> 0</td><td> 1 </td><td></td>
<td>Stck </td>
<td>nach der Mahlzeit </td>
<td>erhöhte Blutfette</td>
</tr>
<tr>
<td styleCode='Bold'>Anwendung unter die Haut</td>
</tr>
<tr>
<td>Insulin </td>
<td>human Insulin B. Braun Basal</td>
<td> </td>
<td>Spritze </td>
<td>20</td><td> 0 </td><td>10 </td><td></td>
<td>IE </td><td>sub cutan </td><td>Diabetes</td>
</tr>
<tr>
<td styleCode='Bold'>Bedarfsmedikation</td>
</tr>
<tr>
<td>Glyceroltrinitrat </td>
<td>Corangin® Nitrospray</td>
<td></td>
<td>Spray </td><td></td><td></td><td></td><td></td>
<td>max. 3 Hübe </td>
<td>akut </td>
<td>Herzschmerzen</td>
</tr>
<tr>
<td></td>
<td>Vivinox® stark </td>
<td></td>
<td>Tab</td>
<td>0 </td><td>0 </td><td>0 </td><td>1 </td>
<td>Stck </td>
<td>bei Bedarf</td>
<td>Schlaflosigkeit</td>
</tr>
</tbody>
</table>
</text>
<entry>
<observation classCode='OBS' moodCode='EVN' negationInd=' false'>
<code code='xxxx' displayName='xxxx' codeSystem='2.16.840.1.113883.6.96'
codeSystemName='SNOMED CT'/>
<statusCode code='completed'/>
<effectiveTime><low value='20130430'/><high value='20130430'/></effectiveTime>
<value xsi:type='ST' >MP|12.12.2012|1|1|n|
Michaela Mustermann|13.12.1936|
Dr. Manfred Überall|Hauptstraße 55|01234 Am Ort|04562-12345|m.ueberall@mein-netz.de|
4213891|Tab|100|Stck|während der Mahlzeiten|Bluthochdruck|
1167417|Tab|100|Stck|während der Mahlzeiten|Bluthochdruck|
4129423|Tab|001|Stck|während der Mahlzeiten|art. Verschluss|
1048871|Tab|001|Stck|nach der Mahlzeit|erhöhte Blutfette|
#416|
1058964|Spritze|20-0-10|IE|sub cutan|Diabetes|
#Bedarfsmedikation|
3842722|Spray|max. 3|Hübe|akut|Herzschmerzen|
2083906|Tab|0001|Stck|bei Bedarf|Schlaflosigkeit|
¦422|Bitte messen Sie Ihren Blutdruck täglich!|
013|DE</value>
</observation>
</entry>
</section>
</component>
<component>
<section>
<code code="xxxxxx" codeSystem="2.16.840.1.113883.6.1" codeSystemName="LOINC"/>
<title>Wichtige Angaben</title>
<text>
Bitte messen Sie Ihren Blutdruck täglich!
</text>
</section>
</component>
</structuredBody>
</component>
</ClinicalDocument>
Dieses Material ist Teil des Leitfadens Implementierungsleitfaden.
|
Anhang
Felder aus dem AKdÄ-Medikationsplan (1.3)
| Feld- code | Bezeichnung Datenfeld | Syntax | Feldlänge und zulässige Werte | Instanz kommt aus der Datenquelle | Identität zu Ausdruck |
|---|---|---|---|---|---|
| 1.1 | Identifikation | "MP" | fix | Anlage 2 | entsprechend |
| 1.2 | Seite von | X | Länge: 1 Zahl Werte: \[1,2,3\] | Software | absolut identisch mit Ausdruck |
| 1.3 | Gesamtseitenzahl | Y | Länge: 1 Zahl Werte: \[1,2,3\] | Software absolut identisch mit Ausdruck | |
| 1.5 | Zertifizierungsstatus | X | 1 Zeichen
"j" oder "n" für ja oder nein||Software||Entsprechend dem Zertifizierungslogo(1.4) | ||
| 2.1 | Patientenname | Freitext | Länge: 1 – 40 | Zeichen | Software absolut identisch mit Ausdruck |
| 2.2 | Geburtsdatum des Patienten | TTMM(j)JJJ | Länge: 9 Zeichen
Werte >01.01.1890||Software ||inhalt identisch,Format angepasst | ||
| 2.3 | Ersteller des MP | Freitext | Länge: 0 - 25 Zeichen | Software | absolut identisch mit Ausdruck |
| 2.4 | Datum der Erstellung | TTMM((jj)JJ | Länge: 8 Zeichen
Werte >=01.07.2012||Software ||inhalt identisch, Format angepasst. | ||
| 2.5 | Kontaktdaten der Erstellers | Freitext | Länge: 0 – 50 Zeichen | Software | absolut identisch mit Ausdruck |
| 2.6 | Sonstige Angaben | Freitext | Länge: 0 – 50 Zeichen | Software, Schlüsselworte von Anlage 2 | absolut identisch mit Ausdruck |
| 3.1 | Wirkstoffname | bleibt leer, wenn Arzneimittel über PZN eindeutig identifiziert. | über PZN eindeutig zuordenbar | ||
| ATC: mindestens5 stellig |
Länge: 5 – 8 Zeichen Werte: ATC-Code |
akueller ATC laut Anlage 1 | Die Wirkstoffbezeichnung ist dem ATC-Code entsprechend; Es ist keine PZN verfügbar. | ||
| Freitext | Länge: 0 - 30 Zeichen | Anwender gibt Wert über Software ein | Absolut identisch; es ist keine PZN noch ATC-Code verfügbar. | ||
| 3.2 | Handelsname | PZN (ab 1.1.13: PZN-8) |
Länge: 7(8 Ziffern) | AM-Datenbanken, entsprechend der Fachinformation, AMG §11a | Entsprechend |
| Freitext | Länge: 0 - 40 Zeichen | Anwender gibt Wert über Software ein | absolut identisch mit Ausdruck | ||
| 3.3 | Wirkstärke | bleibt leer, wenn Arzneimittel über PZN eindeutig identifiziert. | über PZN eindeutig zuordenbar | ||
| Freitext | Länge: 0 – 8 Zeichen | Anwender gibt Wert über Software ein | absolut identisch mit Ausdruck | ||
| 3.4 | Darreichungsform | Freitext | Länge: 0 – 7 Zeichen | Anwender gibt Wert über Software ein | absolut identisch mit Ausdruck |
| 3.5 | Dosierschema | Freitext | Länge: 0 – 10 Zeichen | Anwender gibt Werte über Software ein | absolut identisch mit Ausdruck |
| Form "XYZ" | Länge: 3 Zeichen Werte: \[0 .. 9,1/2,1/4,-\] |
Anwender gibt Wert über Software ein | entsprechend, andere Formatierung | ||
| Form "WXYZ" | Länge: 4 Zeichen Werte: \[0 .. 9,1/2,1/4,-\] | Anwender gibt Wert über Software ein entsprechend, | andere Formatierung | ||
| 3.6 | Dosierungseinheit | Freitext | Länge: 0 – 7Zeichen | Anwender gibt Wert über Software ein | absolut identisch mit Ausdruck |
| 3.7 | Hinweise | Freitext | Länge: 0 - 35 Zeichen | Anwender gibt Wert über Software ein, wird ggf. durch die Software unterstützt | absolut identisch mit Ausdruck |
| 3.8 | Behandlungsgrund | Freitext | Länge: 0 – 25 Zeichen | Anwender gibt Wert über Software ein, wird ggf. durch die Software unterstützt | absolut identisch mit Ausdruck |
| 4.1 | Zwischenüberschrift mit Kennung | "\#" + Freitext | Länge: 0 – 31 Zeichen | Entweder Anhang B oder vom Anwender oder der Software vorgegeben. | identisch, "\#" ist die Kennung, dass es sich um eine Zwischen-überschrift handelt |
| \#xyz | Länge: 4 Zeichen Werte: xyz sind Ziffern nur aus dem Codebereich 41z zulässig. | Anlage 2 | Text-Code-Tabelle aus Anlage 2 | ||
| 4.2 | Überschrift | X | Länge: 1 Zeichen Wert: "¦" | Durch den Anwender gesetzt, Anlage 2 | Entsprechend |
| 4.3 | Sonstige Hinweise | Freitext | Länge: 0 – 200 Zeichen | Anwender gibt Wert über Software ein | absolut identisch mit Ausdruck |
| 5.1 | Versionsnummer der Spezifikation | (X)XY | Länge: 2 – 3 Ziffern | ist in der Software hinterlegt | Entsprechend,andere Formatierung |
| 5.2 | Datum der Version | Wird nicht im Barcode genutzt. | |||
| 5.3 | Länderkennzeichen | XY | Länge: 2 Zeichen Wert: "DE" | wird von der Software Automatisch gesetzt, Anlage 1 und 2 | absolut identisch mit Ausdruck |
| 5.4 | Herstellerangabe | Nicht im Barcode enthalten; obliegt dem Hersteller, wie dieses Feld zu füllen ist. | Ohne Entsprechung, kein Transfer im 2DBarcode notwendig | ||
| 5.5 | Freifeld | ohne Entsprechung |
Felder aus dem AKdÄ-Medikationsplan (2.0)
|
|
Es gibt hier fundamentale Unterschiede zu vorhergehenden Versionen. |
offene Punkte
- Klärung der notwendigen Headerelemente
- Ausspezifikation der Sektionen und des Entries
- LOINC-Codes
- beautifying des XML-Beispiels
- ...
Referenzen
http://www.akdae.de/AMTS/Massnahmen/docs/Medikationsplan.pdf