Medikationsplan ePA
|
|
Das vorliegende Dokument wird im Rahmen des Forschungs- und Entwicklungsprojekt "Elektronische Patientenakte gemäß § 291a SGB V" erarbeitet. Die im HL7-Wiki bereitgestellte Version dient auch der Entwicklung einer einheitlichen Vorgehensweise zur Spezifikation von Inhalten einer elektronischen Patientenakte. Zum aktuellen Zeitpunkt haben die hier wiedergegebenen Inhalte keinerlei normativen Charakter. Sie stellen keine Vorgaben für Implementierungen außerhalb des FuE-Projektes dar. Weitere Details und Projektergebnisse werden auf der Projektwebseite bereitgestellt. Kommentare zum Inhalt oder zur Vorgehensweise sind willkommen. |
|
|
This article or section is in the middle of an expansion or major restructuring and is not yet ready for use. You are welcome to assist in its construction by editing it as well. If this article has not been edited in several days, please remove this template. This article was last edited by Wikiadmin (talk| contribs) 9 years ago. (Purge) Diese Seite oder Abschnitt ist derzeit ein Entwurf und ist noch nicht fertiggestellt. Du bist eingeladen, bei der Fertigstellung mitzuwirken. Wenn dieser Beitrag länger als einige Tage nicht editiert wurde, entferne diese Vorlage. This article was last edited by Wikiadmin (talk| contribs) 9 years ago. (Purge) |
|
|
Dieses Dokument gibt wieder:
Implementierungsleitfaden Medikationsplan ePA (0.9). Die Teilmaterialien gehören der Kategorie cdaxxxx an. |
HL7 Clinical Document Architecture Release 2
für das deutsche Gesundheitswesen
.
| Abstimmungsdokument | |||
|---|---|---|---|
| Version | Datum | Status | Realm |
| 01 | ??.??.2013 | ||
| noch kein download verfügbar | |||
| Kontributoren | ||
|---|---|---|
| 100px | TMF | Berlin |
Inhaltsverzeichnis
- 1 Einleitung
- 2 Informationsmodell und Anforderungen
- 3 Implementierung
- 4 Regeln für das Dokument
- 5 Regeln für Abschnitte im CDA-Body (Sections)
- 6 Regeln für eingebettete strukturierte Datenelemente (Entries)
- 7 Vokabular
- 8 Konformanz
- 9 Werkzeuge zur Erstellung, Validierung und Darstellung
- 10 Verwendete Templates
- 11 Literatur
- 12 Referenzen
Einleitung
Das Dokument beschreibt die Implementierungsregeln für den Medikationsplan im Rahmen der elektronischen Patientenakte (ePA). Um eine breite Akzeptanz herzustellen, dient der Implementierungsleitfaden des Arztbriefes für das deutsche Gesundheitswesen als Referenz [1]. Insbesondere Kap. 1-3 des IG Arztbrief stellen die Grundlage für viele Elemente des Medikationsplans dar. Auf diese Kapitel wird aus Gründen der Redundanzvermeidung hier nicht detailliert eingegangen.
Informationsmodell und Anforderungen
Der Fokus des Implementierungsleitfadens liegt auf der Beschreibung der zum Austausch und Speicherung benötigten Medikationspläne in Form von CDA Dokumenten.
|
|
Inhalte liegen vor und werden demnächst hier eingearbeitet Christof Gessner 13:21, 20. Mär. 2012 (CET) |
Implementierung
Clinical Document Architecture
Grundlage dieser Spezifikation ist die HL7 Clinical Document Architecture CDA® Release 2.
Allgemeine Regeln für den CDA Header
Grundlagen und allgemeine Regeln für den Header sind im Dokument CDA-Header angegeben.
|
|
Vorgehensweise für CDA-Header abstimmen. Christof Gessner 13:21, 20. Mär. 2012 (CET) |
Weitere verwendete Standards und Templates
Es werden Elemente aus den folgenden Spezifikationen verwendet:
- Smart Open Services for European Patients [2]
- IHE PCC Medical Documents Specification (1.3.6.1.4.1.19376.1.5.3.1.1.1)
- HL7 Implementation Guide for CDA Release 2: History and Physical (H&P) Notes (U.S. Realm) DSTU Release 1, 2008-07-16
- ASTM/HL7 Continuity of Care Document (CCD)
- HL7 Implementation Guide for CDA® Release 2: IHE Health Story Consolidation, Release 1 (DSTU December 2011)
Eine Grundvoraussetzung ist es, dass klinische Dokumente valide sein müssen bezüglich der entsprechenden XML-Schemata. Bei einer Spezialisierung klinischer Dokumente für verschiedene fachliche Kontexte wie beispielsweise der Spezialisierung zum Medikationsplan werden die möglichen Strukturen und Inhalte weiter eingeschränkt. Das technische Mittel zur Einschränkung sind sogenannte Templates, welche zusätzliche Validierungsregeln in Form von Schematron-Regeln definieren und innerhalb des CDA-Dokuments über das templateId-Element referenziert werden.
Regeln für das Dokument
Regeln für den CDA Header im Medikationsplan
Zusätzlich zu den allgemeinen Regeln für den CDA-Header gelten folgende Regeln und Einschränkungen: ...tbd...
|
|
Inhalte liegen vor und werden demnächst hier eingearbeitet Christof Gessner 13:21, 20. Mär. 2012 (CET) |
Regeln für den Inhalt des CDA-Body im Medikationsplan
Im Kontext des Medikationsplans enthält ein CDA Dokument einen strukturierten CDA-Body. Der CDA-Body enthält lediglich eine Sektion mit dem LOINC Code für Medikation und dem Titel „Medikationsplan“.
10160-0 (LOINC) HISTORY OF MEDICATION USE
Das folgende Fragment zeigt die Grobstruktur eines CDA-Medikationsplans.
<ClinicalDocument
xmlns="urn:hl7-org:v3"
xmlns:xsi="http://www.w3.org/2001/XMLSchema-instance">
<typeId root="2.16.840.1.113883.1.3" extension="POCD_HD000040"/>
<!--CDA Header -->
...
<!--CDA Body -->
<component>
<structuredBody>
<component>
<section>
<templateId root="2.16.840.1.113883.10.20.1.8"/>
<templateId root="1.3.6.1.4.1.19376.1.5.3.1.3.19"/>
<templateId root="1.3.6.1.4.1.12559.11.10.1.3.1.2.3"/>
<code code="10160-0"
codeSystem="2.16.840.1.113883.6.1"
codeSystemName="LOINC"
displayName="HISTORY OF MEDICATION USE"/>
<title="Medikationsplan"/>
...
</section>
</component>
</structuredBody>
</component>
</ClinicalDocument>
Regeln für Abschnitte im CDA-Body (Sections)
Regeln für den Abschnitt Medikationsplan (Section)
Verwendete Section level templates
Folgende Templates werden verwendet:
epSOS medication summary section template (1.3.6.1.4.1.12559.11.10.1.3.1.2.3) Parent Templates:
- CCD 3.9 (2.16.840.1.113883.10.20.1.8)
- IHE PCC, Volume 2, Revision 5 (1.3.6.1.4.1.19376.1.5.3.1.3.19)
- epSOS Medication Summary Section 1.3.6.1.4.1.12559.11.10.1.3.1.2.3
Attribute und Relationen
required: Section.code = 10160-0 (LOINC) HISTORY OF MEDICATION USE
required: title="Medikationsplan"
Die Section soll einen eindeutigen Identifikator haben (id).
Die Section enthält keine weiteren Komponenten (component).
Für die Section sind keine Relationen enthalten (author, informant, subject). Somit gelten die im CDA-Header bzw. in einer ggf. einschließenden Section gegebenen Relationen.
Narrativer Teil
Im narrativen Teil wird die Medikation in einer Tabelle strukturiert angegeben, deren Form und Inhalt angelehnt ist an die Vorgaben des Aktionsbündnisses AMTS.
Strukturierte Elemente (CDA Level 3)
Die Section Medikationsplan enthält ein oder mehrere Entries "Medikament und Dosierung (SubstanceAdministration mit epSOS-Erweiterungen)".
required: entry 1.3.6.1.4.1.12559.11.10.1.3.1.3.4 (Medication Item)
Beispiel:
<section>
<!-- CCD 3.9 Medication section template -->
<templateId root="2.16.840.1.113883.10.20.1.8"/>
<!-- PCC Medication section template -->
<templateId root="1.3.6.1.4.1.19376.1.5.3.1.3.19"/>
<!-- epSOS medication summary section template -->
<templateId root="1.3.6.1.4.1.12559.11.10.1.3.1.2.3"/>
<id root="bd8a953a-761d-4136-95fc-5146223ef060"/>
<!—Section type according LOINC -->
<code code="10160-0"
codeSystem="2.16.840.1.113883.6.1"
codeSystemName="LOINC"
displayName="HISTORY OF MEDICATION USE"/>
<title>Medikationsplan</title>
<text> ... </text>
<entry>
<substanceAdministration classCode='SBADM' moodCode='EVN'>
<templateId root='1.3.6.1.4.1.12559.11.10.1.3.1.3.4'/>
...
</substanceAdministration>
</entry>
</section>
Regeln für eingebettete strukturierte Datenelemente (Entries)
Medikament und Dosierung (Arztbrief bvitg)
Die Angaben von Medikamenten, die ein Patient eingenommen hat, einnimmt oder einnehmen soll, werden in den in Deutschland verbreiteten Informationssystemen in der Regel als Freitext erfasst. Informationen zu Medikation umfassen
- die Beschreibung des Medikaments und seiner Darreichungsform,
- Angaben zur Dosierung,
- Zeitangaben für die Einnahme und
- Verabreichungsanweisungen.
Strukturierte Erfassungen der Dosierungen oder codierte Angaben zur Beschreibung des Medikaments sind noch eher die Ausnahme. Praxisinformationssysteme verwenden zur Klassifikation eines Medikaments in der Regel die Pharmazentralnummer (PZN). Für Zeitangaben ist es meist üblich, Tagesschemata anzugeben, wie 1-0-1 für morgens 1x, abends 1x etc. Verabreichungsanweisungen werden, wenn überhaupt, im Klartext erfasst und kommuniziert.
Die im Medikationsplan erforderlichen Angaben beinhalten Daten zur Dosierung und Einnahmedauer. Die verwendete Arznei wird mit Hilfe der consumable-Participation festgelegt und kann sich auf Wirkstoff (Substanzen) oder reguläre Medikamente (Produkte) beziehen.
Als eindeutige Nummer, die Arzneimittel hinsichtlich Wirkstoff, Wirkstärke, Darreichungsform, Anbieter und Packungsgröße identifiziert, ist die PZN im deutschen Markt konkurrenzlos.(Quelle: [3])
Beispiel aus dem Addendum "Medikation" zum bvitg-Artzbrief:
<substanceAdministration classCode="SBADM" moodCode="EVN">
<id extension="v44285637" root="1.2.276.0.76.1210.23.27.123"/>
<text>Atemur mite 50, morgens 2x und abends 1x bei Bedarf inhalieren</text>
<priorityCode code="PRN" codeSystem="2.16.840.1.113883.5.7"/>
<routeCode code="ORINHL" codeSystem="2.16.840.1.113883.5.112"
codeSystemName="RouteOfAdministration"
displayName="Inhalation, oral"/>
<consumable>
<manufacturedProduct>
<manufacturedLabeledDrug>
<code code="7126336" codeSystem="1.2.276.0.76.4.6"
codeSystemName="Pharmazentralnummer"
displayName="ATEMUR mite 50 Dos.Aerosol 120 ED 1 St"/>
</manufacturedLabeledDrug>
</manufacturedProduct>
</consumable>
</substanceAdministration>
Beispiel zur Codierung des Wirkstoffes mit ATC als translation der PZN-Nummer (zusätzlich ist zur Veranschaulichung eine weitere Kodierung als translation angegeben):
<consumable>
<manufacturedProduct>
<manufacturedLabeledDrug>
<code code="7621113" codeSystem="1.2.276.0.76.4.6"
codeSystemName="Pharmazentralnummer"
displayName="Aspirin(R) 100">
<translation
code="B01AC06" codeSystem="1.2.276.0.76.5.320"
codeSystemName="ATC GM 2007"/>
<translation
code="E00228C.F00016D.W00022F.J001155.Z100002.Z200001-ab7621113-54"
codeSystem="1.2.276.0.76.5.305"
codeSystemName="IDMACS"/>
</code>
</manufacturedLabeledDrug>
</manufacturedProduct>
</consumable>
Im Addendum "Medikation" zum bvitg-Artzbrief finden sich zahlreiche Beispiele und Erläuterungen zum Umgang mit Dosierungs- und Zeitangaben und Verabreichungsanweisungen.
Im folgenden ein Beispiel (aus der epSOS-Spezifikation) mit verschiedenen entryRelationships. Auf diese Weise können innerhalb eines SubstanceAdministration Entries auch komplexere Sachverhalte dargestellt werden, wie etwa Verabreichungsanweisungen.
(Anmerkung: zur besseren Übersicht sind in diesem Beispiel viele Attributwerte weggelassen worden)
<substanceAdministration classCode='SBADM' moodCode='EVN'>
<templateId root='2.16.840.1.113883.10.20.1.24'/>
<templateId root='1.3.6.1.4.1.19376.1.5.3.1.4.7'/>
<templateId root='1.3.6.1.4.1.12559.11.10.1.3.1.3.4'/>
<id root='' extension=''/>
<code code='' codeSystem='' displayName='' codeSystemName=''/>
<text>
<reference value='#med-1'/>
</text>
<statusCode code='completed'/>
<effectiveTime xsi:type='IVL_TS'>
<low value=''/>
<high value=''/>
</effectiveTime>
<effectiveTime operator='A' xsi:type='TS|PIVL_TS|EIVL_TS|PIVL_PPD_TS|SXPR_TS'>
...
</effectiveTime>
<routeCode code='' codeSystem='' displayName='' codeSystemName=''/>
<doseQuantity value='' unit=''/>
<approachSiteCode code='' codeSystem='' displayName='' codeSystemName=''/>
<rateQuantity value='' unit=''/>
<consumable>
...
</consumable>
<author>
<time/>
<assignedAuthor>
<id/>
<assignedPerson>
<name></name>
</assignedPerson>
</assignedAuthor>
</author>
<!-- 0..* entries describing the components -->
<entryRelationship typeCode='COMP' >
<sequenceNumber value=''/>
</entryRelationship>
<!-- An optional entry relationship that indicates the the reason for use -->
<entryRelationship typeCode='RSON'>
<act classCode='ACT' moodCode='EVN'>
<templateId root='1.3.6.1.4.1.19376.1.5.3.1.4.4.1'/>
<id root='' extension=''/>
</act>
</entryRelationship>
<!-- Optional instructions for Pharmacist -->
<entryRelationship typeCode='SUBJ'>
...
</entryRelationship>
<precondition>
<criterion>
<text><reference value=''></text>
</criterion>
</precondition>
</substanceAdministation>
Value Set für routeCode: epSOSRouteofAdministration, OID: 1.3.6.1.4.1.12559.11.10.1.3.1.42.12 (Codesystem EDQM 1.3.6.1.4.1.12559.11.10.1.3.1.44.1)
Medikament und Dosierung (SubstanceAdministration mit epSOS-Erweiterungen)
IHE PCC Medications Entry content module, 1.3.6.1.4.1.19376.1.5.3.1.4.7
2.16.840.1.113883.10.20.1.24 (CCD) 1.3.6.1.4.1.12559.11.10.1.3.1.3.4 (epSOS)
Dosierungs- und Zeitangaben und Verabreichungsanweisungen können bei Verwendung dieser Extension genauso abgebildet werden wie im Addendum "Medikation" zum vhitg-Arztbrief angegeben und erläutert.
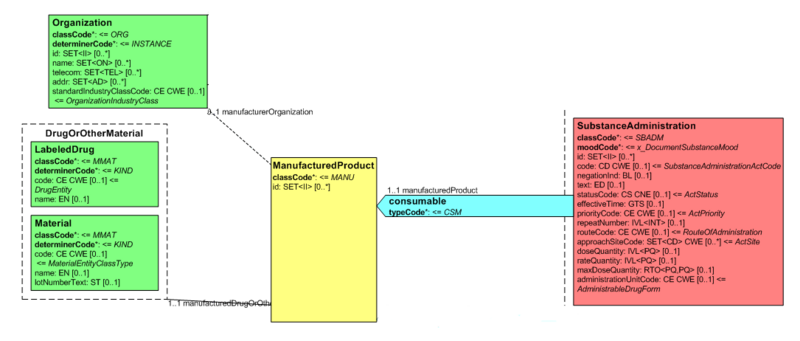
epSOS definiert extensions für das Medicine Entry Content Module (1.3.6.1.4.1.12559.11.10.1.3.1.3.1). Dabei werden einzelne Elemente verwendet aus dem HL7 V3 R_Medication Universal Common Message Element (CMET), Release 2 aus der HL7 V3 2009 Normative Edition (COCT_RM230100UV).
Die benötigten Elemente aus dem CMET werden als zusätzliche Elemente unter manufacturedMaterial verwendet. Der Vorteil dieser Extension liegt in den umfassenderen Möglichkeiten, ein pharmazeutisches Produkt auf mehreren Ebenen (Packung, Wirkstoff) konsistent zu beschreiben. Darüber hinaus soll so die Konsistenz mit den auf europäischer Ebene entwickelten epSOS-Spezifikationen sichergestellt werden. Diese CDA-Erweiterung ist konform zu den Vorgaben in Kapitel 1.4 CDA Extensibility der CDA-Spezifikation.
|
|
Eine Abbildung auf die "herkömmlichen" CDA-Strukturen unter Verzicht auf die hier beschriebene Extension erscheint im Hinblick auf Anwendungsszenarien des Medikationsplans aber auch möglich. |
Für diese Elemente dieser extension wird der folgende Namespace verwendet: urn:epsos-org:ep:medication
Hier die Darstellung aus der epSOS-Spezifikation (D3.9.1 - Appendix B1: epSOS Semantic Implementation Guidelines):
<consumable>
<manufacturedProduct xmlns:epsos="urn:epsos-org:ep:medication"classCode="MANU">
<templateId root="1.3.6.1.4.1.12559.11.10.1.3.1.3.1"/>
<manufacturedMaterial classCode="MMAT" determinerCode="KIND">
<!-- National medicinal product code -->
<code code=" " displayName="Pyrimon" codeSystem=" "codeSystemName=" "/>
<!-- Brand name -->
<name>Pyrimon</name>
<epsos:formCode code="10604000" displayName="Eye drops, solution"
codeSystem="1.3.6.1.4.1.12559.11.10.1.3.1.44.1"
codeSystemName="EDQM"/>
<!-- Container information -->
<epsos:asContent classCode="CONT">
<epsos:containerPackagedMedicine classCode="CONT" determinerCode="INSTANCE">
<epsos:name>Pyrimon 5 ml Eye Drops</epsos:name>
<epsos:formCode
code="30008000" displayName="Bottle" codeSystem="1.3.6.1.4.1.12559.11.10.1.3.1.44.1"
codeSystemName="EDQM"/>
<epsos:capacityQuantity value="5" unit="ml"/>
<epsos:capTypeCode code="30022000" codeSystem=" 1.3.6.1.4.1.12559.11.10.1.3.1.44.1"
displayName="Dropper applicator" codeSystemName="EDQM"/>
</epsos:containerPackagedMedicine>
</epsos:asContent>
<!-- This is the generic equivalent -->
<epsos:asSpecializedKind classCode="GRIC">
<epsos:generalizedMedicineClass classCode="MMAT">
<epsos:code nullFlavor="NA"/>
<epsos:name>Chloramphenicol/ Dexamethasone</epsos:name>
</epsos:generalizedMedicineClass>
</epsos:asSpecializedKind>
<!-- This is the list of active ingredients -->
<epsos:ingredient classCode="ACTI">
<!-- Strength 1% w/v -->
<epsos:quantity>
<epsos:numerator xsi:type="epsos:PQ" value="10" unit="mg"/>
<epsos:denominator xsi:type="epsos:PQ" value="1" unit="ml"/>
</epsos:quantity>
<epsos:ingredient classCode="MMAT" determinerCode="KIND">
<epsos:code code="S01AA01" codeSystem="1.3.6.1.4.1.12559.11.10.1.3.1.44.1"
displayName="chloramphenicol"/>
<epsos:name>Chloramphenicol</epsos:name>
</epsos:ingredient>
</epsos:ingredient>
<epsos:ingredient classCode="ACTI">
<!-- Strength 0.1% w/v -->
<epsos:quantity>
<epsos:numerator xsi:type="epsos:PQ" value="1" unit="mg"/>
<epsos:denominator xsi:type="epsos:PQ" value="1" unit="ml"/>
</epsos:quantity>
<epsos:ingredient classCode="MMAT" determinerCode="KIND">
<epsos:code code="D07CB04" codeSystem="1.3.6.1.4.1.12559.11.10.1.3.1.44.1"
displayName="dexamethasone and antibiotics"/>
<epsos:name>Dexamethasone</epsos:name>
</epsos:ingredient>
</epsos:ingredient>
</manufacturedMaterial>
</manufacturedProduct>
</consumable>
Darreichungsform (epSOS Extension)
<epsos:formCode code="10604000" displayName="Eye drops, solution"
codeSystem="1.3.6.1.4.1.12559.11.10.1.3.1.44.1"
codeSystemName="EDQM"/>
Value Set für manufacturedMaterial.formCode: epSOSDoseForm, OID: 1.3.6.1.4.1.12559.11.10.1.3.1.42.2 (Codesystem EDQM 1.3.6.1.4.1.12559.11.10.1.3.1.44.1)
Der Wert des Attributs manufacturedMaterial.formCode hat Einfluß auf die Einheiten, die in den Dosierungsangaben in substanceAdministration.doseQuantity verwendet werden müssen: "1" für abzählbare Inhalte, extensive Einheiten für nicht-abzählbare Formen wie Pulver, Flüssigkeiten.
ACHTUNG: Dies ist die Darreichungsform ("pharmaceutical dose form"). Die Mengenangabe auf Ebene der Packung (s.u. containerPackagedMedicine) soll sich auf diese Dosierungsform beziehen. Bei bestimmten Produkten ist eine eindeutige Beschreibung hier schwierig. Beispiele: Darreichungsform=Lösung und Produktform=Pulver (das Pulver befindet sich in Tütchen und muss vor Einnahme in Wasser aufgelöst werden: Eine Packung enthält 10 Tütchen, in einem Tütchen sind x mg Pulver mit y mg Wirkstoff, daraus werden 100 ml Lösung zubereitet), Darreichungsform=Lösung und Produktform=Konzentrat in Ampulle (der Inhalt der Ampulle wird vor Injektion mit NaCl-Lösung verdünnt - bezieht sich eine Mengenangabe in ml auf das Konzentrat oder die verdünnte Lösung?). In solchen Fällen sind zur Vermeidung von Mißverständnissen zusätzliche Hinweise zur Darreichung erforderlich.
Packungsinhalt (epSOS Extension)
Das folgende Fragment beschreibt die Paketierung der Arznei. Neben dem Packungsnamen selbst wird die Produktform (containerPackagedMedicine.formCode), in diesem Fall Spritzampullen, und die Chargennummer (lotNumberText) angegeben. Das letzte Element des Fragments beschreibt die Einheiten pro Packung (zwei Einheiten).
<epsos:asContent classCode='CONT'>
<epsos:containerPackagedMedicine xmlns:epsos="urn:epsos-org:ep:medication"
classCode="CONT"
determinerCode="INSTANCE">
<epsos:name>Lovenox 2000UI</epsos:name>
<epsos:formCode code="30003000"
codeSystem="1.3.6.1.4.1.12559.11.10.1.3.1.44.1"
codeSystemName="epSOSPackage"
displayName="Spritzampullen"/>
<epsos:lotNumberText>24681012</epsos:lotNumberText>
<epsos:capacityQuantity value="2" unit="1"/>
</epsos:containerPackagedMedicine>
</epsos:asContent>
containerPackagedMedicine.formCode beschreibt die Form des Produkts in der Packung. Ein Markenname der Packung kann in containerPackagedMedicine.name angegeben werden.
In capacityQuantity wird angegeben, wieviele Einheiten (bzw. welche Menge) der in manufacturedMaterial.formCode beschriebenen Form in der Packung enthalten sind, die durch containerPackagedMedicine.formCode beschrieben ist. Der Wert des Attributs manufacturedMaterial.formCode hat Einfluß auf die Einheiten, die in den Mengenangaben verwendet werden müssen ("1" für abzählbare Inhalte, extensive Einheiten für nicht-abzählbare Formen wie Pulver, Flüssigkeiten).
Value Set für containerPackagedMedicine.formCode: epSOSDoseForm (??), OID: 1.3.6.1.4.1.12559.11.10.1.3.1.42.2 (Codesystem EDQM 1.3.6.1.4.1.12559.11.10.1.3.1.44.1)
Nicht verwendet(??): Value Set für package: epSOSPackage, OID: 1.3.6.1.4.1.12559.11.10.1.3.1.42.3 (Codesystem EDQM 1.3.6.1.4.1.12559.11.10.1.3.1.44.1)
|
|
Klären: wird in FormCode die Darreichungsform des Medikaments (Augentropfen) oder die Packung (Flasche) beschrieben?? |
Im CMET ist hier angegeben "This is the pack in which the medicine is contained." und als ConceptDomain ContainerEntityType. Das steht im Widerspruch zu den Angaben im epSOS Guide 3.9 Appendix B1 epSOS Semantic Implementation Guidelines:
Dort (12.1.2.5.3.3. Medication Packaging) steht: "The value set is (...) epSOSDoseForm, OID 1.3.6.1.4.1.12559.11.10.1.3.1.42.2". In den Beispielen im gleichen Dokument wird an dieser Stelle ein Code angegeben, der im Value Set epSOSPackage steht (aber nicht im Value Set epSOSDoseForm): containerPackagedMedicine.formCode.code="30008000", containerPackagedMedicine.formCode.codeSystem="1.3.6.1.4.1.12559.11.10.1.3.1.44.1"
Inhaltsstoffe (epSOS Extension)
Die eigentliche Substanz wird durch das gekapselte Element ingredient (vom Typ Substance) beschrieben. Hierzu wird die amtliche Fassung des ATC-Codesystems für Deutschland (OID: 1.2.276.0.76.5.319) verwendet.
<epsos:ingredient classCode="ACTI" xmlns:epsos="urn:epsos-org:ep:medication">
<epsos:quantity>
<epsos:numerator xsi:type="epsos:PQ" value="2000" unit="UI"/>
<epsos:denominator xsi:type="epsos:PQ" value="1" unit="mL"/>
</epsos:quantity>
<epsos:ingredient classCode="MMAT" determinerCode="KIND">
<epsos:code
code="B01AB05"
codeSystem="1.2.276.0.76.5.319"
codeSystemName="ATC"
displayName="Enoxaparin" />
</epsos:ingredient>
</epsos:ingredient>
Es können auch mehrere active ingredients angegeben werden.
Die Stärke wird in quantity als Verhältnis von numerator (Zähler) und denominator (Nenner) angegeben.
|
|
Hier besteht noch Klärungsbedarf: |
Im Fall von Tabletten (containerPackagedMedicine.formCode=Blister, manufacturedMaterial.formCode=tablet) wird hier typischerweise die Wirkstoffmenge in einer Tablette in mg (oder UI, oder...) angegeben. Im Fall von flüssigen Lösungen, Gels o.ä. wird typischerweise eine Konzentration angegeben (z.B. mg/ml). In manchen Fällen wird aber auch hier die Wirkstoffmenge bezogen auf die Darreichungsform angegeben: Fertigspritzen zu 2500 Einheiten pro 0,2 ml
Generisches Äquivalent (epSOS Extension)
|
|
Erläuterung folgt alsbald... Christof Gessner 13:21, 20. Mär. 2012 (CET) |
<epsos:asSpecializedKind classCode="GRIC">
<epsos:generalizedMedicineClass classCode="MMAT">
<epsos:code nullFlavor="NA"/>
<epsos:name>Chloramphenicol/ Dexamethasone</epsos:name>
</epsos:generalizedMedicineClass>
</epsos:asSpecializedKind>
Vokabular
Concept Domains
Codesysteme
- LOINC (2.16.840.1.113883.6.1)
- Confidentiality (2.16.840.1.113883.5.25)
- ISCO-08 (1.2.250.1.213.1.1.4.5)
- TimingEvent (2.16.840.1.113883.5.139)
- PZN (1.2.276.0.76.4.6)
- ATC (1.2.276.0.76.5.319)
- AdministrativeGender (2.16.840.1.113883.5.1)
- MaritalStatus (2.16.840.1.113883.5.2)
- ParticipationSignature (2.16.840.1.113883.5.89)
Value Sets
- epSOS:RoutesofAdministration (1.3.6.1.4.1.12559.11.10.1.3.1.42.12)
- epSOS:DoseForm (1.3.6.1.4.1.12559.11.10.1.3.1.42.2)
- epSOS:Package (1.3.6.1.4.1.12559.11.10.1.3.1.42.3)
|
|
In welcher Form und mit welchen Tools werden Value sets bereitgestellt? Christof Gessner 13:21, 20. Mär. 2012 (CET) |
Konformanz
...tbd...
|
|
Inhalte liegen vor und werden demnächst hier eingearbeitet Christof Gessner 13:21, 20. Mär. 2012 (CET) |
Werkzeuge zur Erstellung, Validierung und Darstellung
Im Rahmen des Projekts wurde ein Stylesheet (XSL) entwickelt, das die Ausgabe konformer CDA-Dokumente "ePA-Medikationsplan" in einem Format ermöglicht, das eng an die vom Aktionsbündnis erarbeiteten Vorschläge angelehnt ist.
Verwendete Templates
- IHE-PCC Medical Document Specification (1.3.6.1.4.1.19376.1.5.3.1.1.1)
- CDAr2 Interoperability Level 3 (2.16.840.1.113883.10.20.30)
- CCD 3.9 (2.16.840.1.113883.10.20.1.8)
- IHE PCC Medications Section (1.3.6.1.4.1.19376.1.5.3.1.3.19)
- epSOS Medication Summary Section (1.3.6.1.4.1.12559.11.10.1.3.1.2.3)
- IHE PCC Medications Entry (1.3.6.1.4.1.19376.1.5.3.1.4.7)
- CCD Medication Item Entry (2.16.840.1.113883.10.20.1.24)
- epSOS Medication Item Entry (1.3.6.1.4.1.12559.11.10.1.3.1.3.4)
- epSOS Normal Dosing (1.3.6.1.4.1.19376.1.5.3.1.4.7.1)
Literatur
- Addendum "Medikation" zum Arztbrief HL7 CDA Release 2, Version 1.00, Stand: 02.07.2007